Температура плавления металлов. Самый тугоплавкий и легкоплавкий металл

Почти все металлы при нормальных условиях представляют собой твердые вещества. Но при определенных температурах они могут изменять свое агрегатное состояние и становиться жидкими. Давайте узнаем, какая температура плавления металла самая высокая? Какая самая низкая?
Температура плавления металлов
Большая часть элементов периодической таблицы относится к металлам. В настоящее время их насчитывается примерно 96. Всем им необходимы разные условия, чтобы превратиться в жидкость.
Порог нагревания твердых кристаллических веществ, превысив который они становятся жидкими, называется температурой плавления. У металлов она колеблется в пределах нескольких тысяч градусов. Многие из них переходят в жидкость при относительно большом нагревании. Благодаря этому они являются распространенным материалом для производства кастрюль, сковородок и других кухонных приборов.
Средние температуры плавления имеют серебро (962 °С), алюминий (660,32 °С), золото (1064,18 °С), никель (1455 °С), платина (1772 °С) и т.д. Выделяют также группу тугоплавких и легкоплавких металлов. Первым, чтобы превратиться в жидкость, нужно больше 2000 градусов Цельсия, вторым – меньше 500 градусов.
К легкоплавким металлам обычно относят олово (232 °C), цинк (419 °C), свинец (327 °C). Однако у некоторых из них температуры могут быть еще ниже. Например, франций и галлий плавятся уже в руке, а цезий можно греть только в ампуле, ведь от кислорода он воспламеняется.

Самые низкие и высокие температуры плавления металлов представлены в таблице:
Самый легкоплавкий металл
Каждый человек множество раз держал в руках самый легкоплавкий металл, причём без всяких последствий. Речь идет о ртути, грозном и загадочном элементе из подгруппы цинка, занимающем в периодической таблице атомный номер 80.
Общие сведения
Название переводится с греческого, как «серебряная вода». На латинском звучит как hydrargyrum, а в русском это толкование праславянского — «катиться». Первая цивилизация шумеров уже вовсю использовала ртуть. Металл добывали из киновари (сульфида ртути) просто обжигая руду, или же из пород, где его видно в виде небольших вкраплений.
Это редкий элемент — общая доля в земных недрах составляет всего 83 мг на одну тонну, причем чаще в рассеянной форме, чем в виде месторождений. Больше всего ее содержится в сульфидах и сланцах, а всего в мире имеется более 20 минералов со ртутью.

Самый легкоплавкий металл
Это единственный из металлов, который может находиться в жидком состоянии при обычной температуре. Такой же и бром, только он относится к галогенам. Твердеет ртуть (и плавится) при -39 °С.
Всего 7 металлов плавятся при минусовой температуре. Литр ртути очень тяжелый — 13,5 кг, а закипит она при +357°С.

Ртуть в природе
Интересно что доказательства ее принадлежности к металлам были опубликованы только в середине XVIII века Брауном и Ломоносовым. Они смогли заморозить ртуть и убедиться в ее металлических свойствах: ковкости, электропроводности, расширении при нагреве.
Самый токсичный металл
Ртути принадлежит высочайшая степень токсичности. Это самый ядовитый из всех нерадиоактивных элементов на планете, который начинает распространять свои пары при комнатной температуре. Если рядом присутствует человек, происходит поражение пищеварения, легких и нервной системы, причём первые признаки интоксикации наступают очень быстро, через 8 часов.
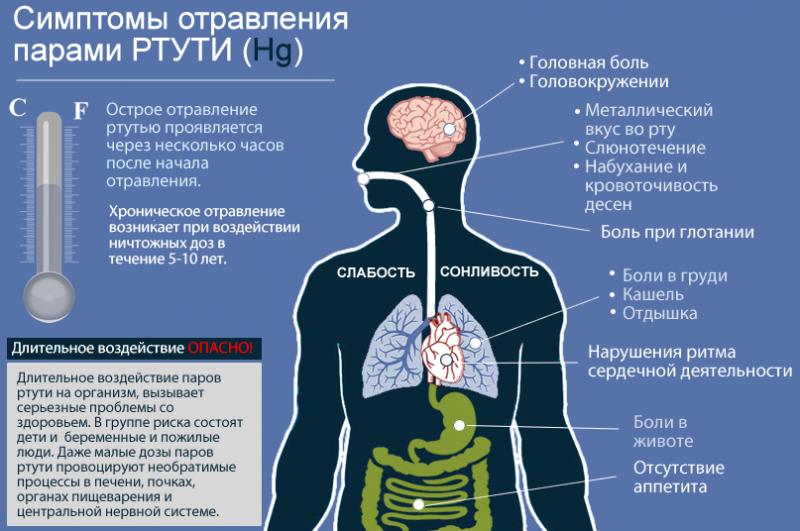
Симптомы отравления ртутью
И даже воздействие небольших доз, но длительный период, способно проявить себя в виде хронических заболеваний. Нервная система в первую очередь реагирует раздражением, недосыпанием, головными болями и быстрой усталостью. Выводится ртуть через почки. Начинаются частые позывы к мочеиспусканию, повышение температуры, рвота, слабость, тошнота, дрожь в теле.
Самая известная экологическая трагедия XX века, болезнь Минамата, вызвана отравлением метилртутью. Промышленное загрязнение бухты этого японского города в 1956 году привело к 3 тыс. жертв.
Люди всегда знали о токсических свойствах ртути. Например, при изготовлении фетровых шляп использовались ртутные соединения, но другого способа тогда не было. У мастеров часто развивались поражения нервной системы и слабоумие. Поэтому безумный Шляпник, описанный Льюисом Кэрроллом в «Алисе в стране чудес», совсем не выдуманный персонаж.

Безумный Шляпник из “Алисы в стране чудес”
В обычной жизни пищевые отравления грозят любителям морепродуктов. Ртуть содержится и растворяется в морской воде, накапливаясь в организмах его обитателей.
Симптомы хронического отравления часто встречаются в прибрежных районах по всему миру. Особенно страдают беременные и дети, у которых это основная пища. Умеренная олигофрения диагностируется там намного чаще, чем у тех групп, где морская рыба не является основным источником питания.
Хищники, поедая мелочь, сохраняют и приумножает отраву в своих организмах. У каждой четвертой выловленной рыбы содержание металла превышает допустимые пределы. Особенно много его в тунце и лобстере. Экологи бьют тревогу, а компании по производству рыбных продуктов открещиваются. И никакая тепловая обработка не делает мясо менее токсичным.
Использование самого легкоплавкого металла в быту
Несмотря на токсичность, человечество до сих пор не может отказаться от ртути.
Хорошая электропроводимость делает ее незаменимой в энергосберегающих лампах, паровых турбинах, вакуумных и диффузных насосах. Умение реагировать на малейшие колебания температуры и давления используется в барометрах и термометрах.
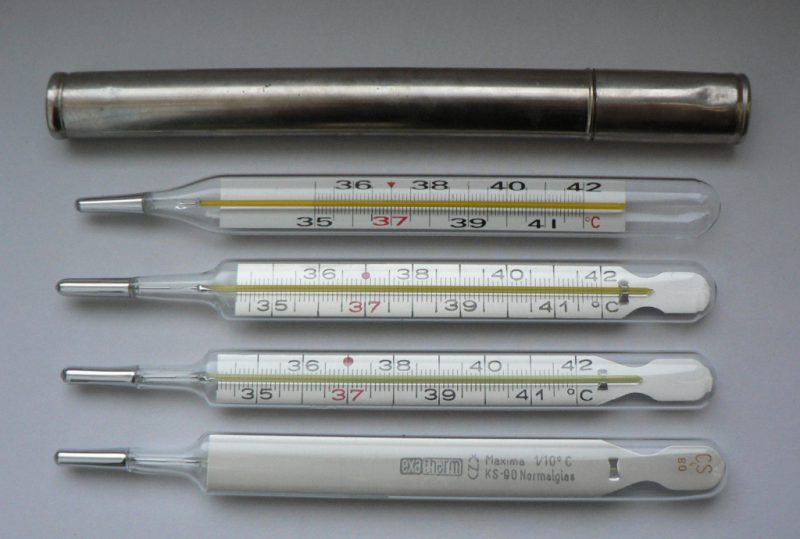
Батарейки, энергосберегающие лампы, аккумуляторы, контакты выключателей — везде содержится этот высокоионизированный металл. В градуснике находится от 1 до 2 гр этого металла (в стандартных российских 1 гр). Но и эти несколько граммов полностью испарятся из помещения только в течение 20 лет. При концентрации менее 0,25 мгм3 ртуть оседает в легких. При более высоких дозах организм начинает впитывать яд через кожу. Мужчины менее чувствительны к парам, чем дети и женщины.

Вы можете найти ртуть в холодильнике, стиральной машине и кондиционере. Сельское хозяйство чаще всего использует соли ртути в составе пестицидов. Взрывчатка содержит фульминат ртути, антисептики — сульфат.

Фульминат ртути (взрывчатое вещество)
Не могут отказаться от ртути при окрашивании бортов корабля. Морские микроорганизмы всегда селятся там и существенно разрушают обшивку. Только краска на основе «серебряной воды» помогает сохранить судно.

Покраска судна
Человечество с самых древних времен использовало ртуть для добычи из руды драгоценных металлов. Ртуть создает сплавы со всеми металлами (амальгамация) и только благодаря ей добыча серебра и золота в Мексике конкистадорами, начиная XVI века, достигла таких впечатляющих размеров и изменила весь мир.

Добыча золота ртутью
Никогда ртуть не транспортируют в самолетах, причем дело не в токсичности. Ртуть хорошо вступает в контакт со всеми металлами, делая их ломкими. Особенно это касается алюминиевых сплавов — случайная авария может повредить самолет.
Использование самого легкоплавкого металла в медицине
Ядовитый металл чаще всего встречался в эликсирах бессмертия и лекарствах для продления жизни. Алхимики пробовали добывать золото прямо из ртути, только сначала ее надо было нагреть. Ртуть называли праматерью металлов, она входила в теорию трех начал (с серой и солью) и была основным элементом философского камня.

Ртуть
Даже магические действия шаманов не могли обойтись без ртути. Распыляемым порошком киновари отпугивали нечистых духов. Несмотря на токсичность, «серебряную воду» активно использовали древние врачи практически во всех сферах своей деятельности.
Древнеегипетские жрецы клали немного ртути в сосуд и помещали в горло фараона, чтобы обезопасить его в загробной жизни.
В Индии йоги пили ртутно-серный напиток и утверждали, что таким образом можно продлить жизнь. Одним из самых вопиющих случаев в древности было лечение заворота кишок с помощью данного химического элемента.
Врачи были уверены, что жидкое серебро должно замечательно проходить сквозь человеческие кишки, распрямляя их. Но данный способ почему-то не прижился, так как у пациентов от большого объема высокоплотного «лекарства» происходил разрыв желудка.
Утверждают, что Иван Грозный стал жертвой именно ртути. Предположительно, ему или лечили сифилис, или давали лекарства, содержащие ртуть. То, что русский царь умер в результате ртутной интоксикации и имел деформации костей, свойственные глубоким старикам, уже доказано несколькими учеными.

Иван Грозный
Историки отмечали, что перед смертью царь очень изменился. Постоянная свирепость, искаженные черты лица, на теле не осталось ни единого волоса. Постоянные эпилептические припадки служили очередным доказательством отравления.
Интересно, что мгновенно покончить с жизнью с помощью ртути ни у кого не получалось. Когда самоубийцы выпивали металл — все они выживали. Самыми опасными являются пары и раствор, а сама ртуть никогда не растворится в желудке и выйдет из организма.
В 70-х годах в продаже можно было встретить множество препаратов с ртутью: мочегонные, слабительные, в мазях для отбеливания лица и антисептиках.
Амальгама серебра не так давно была распространенным пломбировочным стоматологическим материалом в России и до сих пор используется в дешевых пломбах за рубежом.
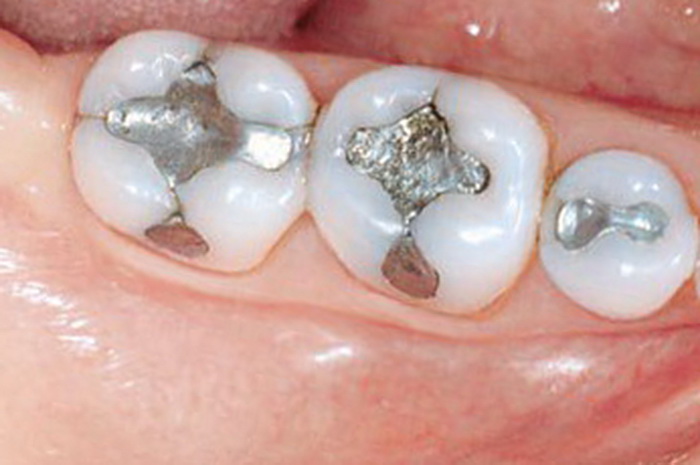
Пломба из амальгамы
Самый легкоплавкий металл на планете необходим человечеству по-прежнему. А вот смогут ли люди дружить с ним, не отравляя жизнь вокруг — очень спорный вопрос…
Самый легкоплавкий металл: свойства и использование
Каждый металл и их сплавы имеют различные свойства. Одно из таких свойств — температура плавления. Каждый металл плавится при разной температуре. Все что нужно для перевода вещества из твёрдого состояния в жидкое — источник тепла, который будет разогревать металл до определенной температуры.
Так как у каждого металла температура плавления различная, можно определить менее устойчивый металл к температуре и более. Так самый легкоплавкий металл — ртуть, он готов перейти в жидкое состоянии при температуре равно 39 градусов по цельсию. А вот вольфрам( из чего собственно и сделаны вольфрамовые электроды для аргоновой сварки), расплавится только по достижению температуры в 3422 градусов цельсии.

Что касается сплавов, таких как сталь и прочих, определить температуру, при которой те будут плавиться, довольно сложно. Вся сложность в их составе… Так как состав разный, то и температура плавления различная. Как правило, для сплавов указывается диапазон температур, при которых он будет плавиться. Вообще, температура плавления металлов интересная тема.
Способы плавления
Читайте также: Особенности обработки деталей на токарно-карусельных полуавтоматах, их технологические возможности.
Способов плавления два — внешний и внутренний. Каждый из способов по своему эффективен. Во время применений внешнего способа плавления, на металл или сплав воздействуют теплом с наружи, на пример в печи. А в случае с внутренним, через металл пропускается высокий разряд электрического тока или воздействуют электромагнитным полем.

На фото индукционный электромагнитный нагреватель металла для кузнечного дела.
Суть понятия самого легкоплавкого металла
Для специалистов больше знакомо понятие «тугоплавкость». Хотя слово «легкоплавки» и является антонимом в языковом аспекте, на практике – это один из пунктов к общей классификации в промышленности. По своей сути, любой элемент, имеющий температуру плавления менее 600 градусов по Цельсию, называют легкоплавким. Некоторые источники ставят планку вхождения в группу еще ниже – до 500 градусов Цельсия.
Классификация металлов по плавкости:
- легкоплавкие. Температура плавления элементов обязана быть ниже 600 градусов по Цельсию;



Процесс плавления одинаковый для всех металлических элементов – либо внешнее воздействие, либо внутреннее. В первом случае – это расплавка в печах, а во втором – разогревание через пропуск электрического тока сквозь металл. Иногда используется индукционный нагрев в электромагнитном поле с высокой частотой.
Процесс плавки металла через призму науки:
- Разогрев до температуры плавления.
- Увеличение амплитуды тепловых колебаний молекул внутри металла.
- Возникновение дефектов в структуре решетки материала.
- Межатомные связи разрываются + параллельно затрачивается энергия.
- Образование на поверхности квазижидкого слоя.
- Постепенное разрушение решетки и накопление дефектов, что и принято называть процессом плавления.
В зависимости от температуры плавления, выбирают аппараты из сплавов, способных выдержать пиковые значения. Для легкоплавких металлов вопрос решается проще всего.
Второй весомый параметр – температура кипения металла. В 95% случаев она в 2 раза выше температуры плавления. Между собой эти две величины являются прямо пропорциональными + при снижении/увеличения давления на материал, снижается и его показатели плавления с кипением.
10 самых крепких металлов в мире
Таблицы плавления металлов и сплавов
Ниже, представлены таблицы, для наглядного знакомства с температурами плавления тех или иных металлов и их сплавов.
Таблица температуры плавления легкоплавких металлов и сплавов
Таблица с температурами плавления легкоплавких металлов
| Название | Обозначение | Плавление | Кипение |
| Олово | Sn | 232°C | 2600°C |
| Свинец | Pb | 327°C | 1750°C |
| Цинк | Zn | 420°C | 907°C |
| Калий | K | 63,6°C | 759°C |
| Натрий | Na | 97,8°C | 883°C |
| Ртуть | Hg | 38,9°C | 356.73°C |
| Цезий | Cs | 28,4°C | 667.5°C |
| Висмут | Bi | 271,4°C | 1564°C |
| Палладий | Pd | 327,5°C | 1749°C |
| Полоний | Po | 254°C | 962°C |
| Кадмий | Cd | 321,07°C | 767°C |
| Рубидий | Rb | 39,3°C | 688°C |
| Галлий | Ga | 29,76°C | 2204°C |
| Индий | In | 156,6°C | 2072°C |
| Таллий | Tl | 304°C | 1473°C |
| Литий | Li | 18,05°C | 1342°C |
Таблица температуры плавления среднеплавких металлов и сплавов
Таблица температур плавления среднеплавких металлов и сплавов
| Название | Обозначение | t Плавления | t Кипения |
| Алюминий | Al | 660°C | 2519°C |
| Германий | Ge | 937°C | 2830°C |
| Магний | Mg | 650°C | 1100°C |
| Серебро | Ag | 960°C | 2180°C |
| Золото | Au | 1063°C | 2660°C |
| Медь | Cu | 1083°C | 2580°C |
| Железо | Fe | 1539°C | 2900°C |
| Кремний | Si | 1415°C | 2350°C |
| Никель | Ni | 1455°C | 2913°C |
| Барий | Ba | 727°C | 1897°C |
| Бериллий | Be | 1287°C | 2471°C |
| Нептуний | Np | 644°C | 3901,85°C |
| Протактиний | Pa | 1572°C | 4027°C |
| Плутоний | Pu | 640°C | 3228°C |
| Актиний | Ac | 1051°C | 3198°C |
| Кальций | Ca | 842°C | 1484°C |
| Радий | Ra | 700°C | 1736,85°C |
| Кобальт | Co | 1495°C | 2927°C |
| Сурьма | Sb | 630,63°C | 1587°C |
| Стронций | Sr | 777°C | 1382°C |
| Уран | U | 1135°C | 4131°C |
| Марганец | Mn | 1246°C | 2061°C |
| Константин | 1260°C | ||
| Дуралюмин | Сплав алюминия, магния, меди и марганца | 650°C | |
| Инвар | Сплав никеля и железа | 1425°C | |
| Латунь | Сплав меди и цинка | 1000°C | |
| Нейзильбер | Сплав меди, цинка и никеля | 1100°C | |
| Нихром | Сплав никеля, хрома, кремния, железа, марганца и алюминия | 1400°C | |
| Сталь | Сплав железа и углерода | 1300°C — 1500°C | |
| Фехраль | Сплав хрома, железа, алюминия, марганца и кремния | 1460°C | |
| Чугун | Сплав железа и углерода | 1100°C — 1300°C |
Таблица температуры плавления тугоплавких металлов и сплавов
Таблица температур плавления тугоплавких металлов и сплавов
| Название | Обозначение | t Плавления °C | t Кипения °C |
| Вольфрам | W | 3420 | 5555 |
| Титан | Ti | 1680 | 3300 |
| Иридий | Ir | 2447 | 4428 |
| Осмий | Os | 3054 | 5012 |
| Платина | Pt | 1769,3 | 3825 |
| Рений | Re | 3186 | 5596 |
| Хром | Cr | 1907 | 2671 |
| Родий | Rh | 1964 | 3695 |
| Рутений | Ru | 2334 | 4150 |
| Гафний | Hf | 2233 | 4603 |
| Тантал | Ta | 3017 | 5458 |
| Технеций | Tc | 2157 | 4265 |
| Торий | Th | 1750 | 4788 |
| Ванадий | V | 1910 | 3407 |
| Цирконий | Zr | 1855 | 4409 |
| Ниобий | Nb | 2477 | 4744 |
| Молибден | Mo | 2623 | 4639 |
| Карбиды гафния | 3890 | ||
| Карбиды ниобия | 3760 | ||
| Карбиды титана | 3150 | ||
| Карбиды циркония | 3530 |



Получение тугоплавких материалов
Основная трудность, встречающаяся при получении тугоплавких металлов и сплавов, это их высокая химическая активность, которая мешает быть элементу в чистом виде.

Установка для получения тугоплавких металлов
Наиболее распространенной технологией получения считается порошковая металлургия. Существует несколько способов получить порошок тугоплавкого металла.
- Восстановление с помощью триоксида водорода. Такой метод включает в себя несколько этапов, оборудование для обработки — это многотрубные печи, с диапазоном температур от 750 до 950 °С. Данный способ применяется для получения молибдена и вольфрама.
- Восстановление водородом из перрената аммония. При температуре около 500 °С, на заключительном этапе, полученный порошок, отделяют от щелочей с помощью кислот и воды. Применяется для получения рения.
- Соли различных металлов также применяются для получения порошка молибдена. Например, используют соль аммония металла и его порошок не более 15% от общей массы. Смесь нагревается до 500-850 °С при помощи инертного газа, а затем технология производства предусматривает провести восстановление водородом при температуре 850 — 1000 °С.

Производство тугоплавких металлов
Полученный этими способами порошок в дальнейшем подвергают к спеканию в специальные формы, для дальнейшей транспортировки и хранения.
На сегодняшний день, эти способы получения чистых тугоплавких металлов продолжают дорабатываться и применяются новые техники извлечения материала из горных пород. С развитием ядерной энергетики, космической отрасли, металлургии, мы в скором времени сможем наблюдать появление новых методов, возможно более дешевых и простых.
Самый тугоплавкий металл в мире расплавили ученые ИЯФ
Тончайший электронный пучок. Скорость – полмиллиметра в секунду. Самый тугоплавкий материал – карбид гафния – поддается за считанные минуты. Сибирские ученые разработали уникальный подход – прямо в электронно-лучевой установке получают карбид из исходных порошкообразных материалов. Тут же материал плавят в готовое изделие, как в 3D принтере. При такой технологии улучшаются и свойства материала. Раньше его синтезировали в огромной печи и только потом делали расплав.
Извержение в жерле вулкана моделируют ученые Академгородка
– При стандартной технологии просто получаются зерна, требуется очень много время, чтобы они соединились друг с другом. Но все равно остается пористость, которая ухудшает свойства конструкционных материалов. А когда мы ударили электронным пучком, металл не просто расплавился, он стал испаряться, это слишком высокое воздействие, а дальше пошла поверхность ровная и гладкая, – рассказывает старший научный сотрудник Института химии твердого тела Алексей Анчаров.
За один сеанс в установке можно изготовить и многослойное изделие – соединить тугоплавкий слой и, например, теплоизоляционный, который защитит от вредного воздействия. Исследование невозможно было бы без уникальной разработки сибирских физиков.
– Обычный электронный пучок чаще всего используется прямой, в нашем случае – пучок поворачивается на 90 градусов, потому что когда идет испарение, мощный поток паров может попадать на катод и вывести его из строя, – поясняет сотрудник Института ядерной физики Юрий Семенов.
Изделия из карбида гафния можно поставить и на промышленный поток, изготовив штампы и трафареты. То есть снизить цену и временные затраты на производство ядерных ректоров, космических ракет и ускорителей.
– Вы сами понимаете, самый высокотемпературный материал находит применение не только в гражданской области. Поэтому в первую очередь он идет на другие применения, тут пока информации нет, – сообщил старший научный сотрудник Института химии твердого тела Алексей Анчаров.
Дальше ученые разработают оптимальные параметры для автоматизации процесса получения и расплава карбида. Есть и конкретное задание – изготовить новый катод для ускорителя ИЯФ. Детали из самого тугоплавкого материала прочнее и долговечнее и сокращают энергозатраты.
Все выпуски новостей телеканала ОТС, а также программы «Итоги недели», «ПАТРИОТ», «Экстренный вызов», «Пешком по Новосибирской области», «ДПС – дорога. Перекресток. Судьба», «От первого лица» выложены на сайте YouTube.
Применение и нахождение в природе
Самый легкоплавкий металл в мире находится в природе очень рассеяно. Общая его концентрация в земной коре составляет примерно 83 мг/т, что делает его довольно редким элементом. В больших количествах он находится в глинистых сланцах и сульфидных минералах, в особенности в сфалеритах и антимонитах. Встречается в ливингстонитах и метациннабаритах.
Несмотря на свою токсичность, ртуть применяется во многих сферах, например, в металлургии, медицине, химической промышленности, машиностроении, электротехнике и даже сельском хозяйстве. Самый легкоплавкий металл подходит для наполнения энергосберегающих ламп, термометров и барометров.
В тяжёлой промышленности вещество используют для ртутнопаровых турбин, вакуумных установок и диффузионных насосов. Им наполняют измерительные приборы, аккумуляторы, сухие батареи. Ртуть участвует в производстве кондиционеров, холодильников и стиральных машин. В сельском хозяйстве её применяют в составе пестицидов.
Свойства ртути
Итак, самый легкоплавкий металл – это ртуть. Для её плавления нужна температура от 234,32 К или -38,83 °С. Кроме неё, при низких температурах плавятся свинец, таллий, галлий, висмут, олово, кадмий. Закипает ртуть при 629,88 К или 356,73 градусов Цельсия, а при 4,155 К ведёт себя как сверхпроводник.
Она обладает серебристо-белым цветом с ярко выраженным блеском. В периодической таблице ей присвоен номер 80. Это единственный металл, который при комнатной температуре находится в жидком состоянии. В твёрдом состоянии она обладает ромбоэдрической решеткой.

Смотреть галерею
Самый легкоплавкий металл малоактивен при небольших температурах. В таких условиях он слабо реагирует на окислительные растворы и многие газы. Не вступает в реакцию он и с кислородом воздуха, хотя прекрасно растворяется в царской водке.
С другими металлами ртуть образует различные сплавы, амальгамы. С органическими соединениями образует очень прочные связи. С хлором или йодом соединяется после нагревания, образуя ядовитые и практически не диссоциирующие вещества.
Источник https://www.syl.ru/article/374078/temperatura-plavleniya-metallov-samyiy-tugoplavkiy-i-legkoplavkiy-metall
Источник https://topkin.ru/interest/samyiy-legkoplavkiy-metall/
Источник https://msmetall.ru/stanki/samyj-trudno-plavkij-metall.html