В.№39: Восстановление марганца, кремния, фосфора и др. элементов в доменной печи.
Марганец в доменную печь попадает либо в составе агломерата в виде силикатов марганца MnO-SiO2; (MnO)2-SiO2, либо с марганцевой или железной рудой, которые загружают в печь при выплавке чугуна с высоким содержанием марганца. Марганец в состав руд входит в виде оксидов MnO2, Mn2O3, Mn3O4. Высшие оксиды марганца довольно легко восстанавливаются доменными газами при умеренных температурах на колошнике доменной печи до MnO по следующим реакциям:
2Мп02 + СО = Mn2O3 + CO2 — 227556 Дж;
ЗМп203 + СО = 2Mn304 + CO2- 170270 Дж;
Mn3O4 + СО = ЗМпО + CO2 — 52080 Дж.
Эти реакции протекают с выделением большого, количества тепла. Процесс восстановления марганца из MnO по реакции МпО+С = Мп+СО+288288 Дж протекает с поглощением тепла. В доменной печи возможно образование и карбида марганца: ЗМпО + 4С=Мп3С+ЗСО. В присутствии железа процесс восстановления марганца протекает при 1100—1300 °С. Большая часть марганца в виде силиката MnO-SiO2 переходит в шлак, но благодаря наличию извести, стремящейся соединиться с кремнеземом, восстановление марганца из шлака углеродом возможно и протекает по реакции Mn0-Si02+Ca0+C = =Mn + CaO-SiO2+CO+229068 Дж. Степень восстановления марганца составляет при выплавке обычных чугунов ~50 %, а при выплавке марганцовистых ферросплавов 70 %. Марганец теряется частично в виде оксидов в шлаке, частично улетучивается с доменным газом. Для максимального извлечения марганца из шихтовых материалов необходимо обеспечивать дополнительных приход тепла в печь, для чего повышают расход кокса, температуру дутья. Применяют дутье, обогащенное кислородом, повышают содержание извести в шлаках. Содержание марганца в литейном чугуне 0,5—1,3 %, а в передельном 0,5—1,5 %. Содержание марганца в передельном чугуне зависит от содержания серы, поскольку марганец способствует удалению серы из чугуна. При работе на сернистом коксе содержание марганца повышают до 1,0 %, а при работе на низкосернистом коксе в чугуне может быть 0,25—0,50 % Mn. Для доменщиков выгодно выплавлять чугун с пониженным содержанием марганца, так как это позволяет экономить кокс, повышает производительность печи и снижает себестоимость чугуна. Однако для успешного хода кислородно-конвертерного процесса требуется чугун с содержанием 0,7—1,1 % марганца. Помимо обычных чугунов, в случае необходимости в доменной печи можно выплавлять ферромарганец с 70—75 % марганца, зеркальный чугун с содержанием марганца 10—25 %. Для выплавки этих сплавов в шихту дают марганцевую руду или марганцевый агломерат, повышают расход кокса до 1000 кг/т зеркального чугуна и 2000 кг/т ферромарганца. Дутье обогащают кислородом до 30—35 %. Это снижает высокую температуру на колошнике печи, помогает уменьшить потери марганца в результате его испарения, уменьшает на 20—30 % расход кокса.
Восстановление кремния
Кремний попадает в доменную печь либо в виде кремнезема SiO2, либо в виде силикатов^, (соединений кремнезема с другими оксидами) в составе железной руды или агломерата, золы кокса, известяка. Кремний имеет сродство к кислороду значительно более высокое, чем железо, поэтому кремний восстанавливается по реакции прямого восстановления: Si02-f2C — Si + 2C0-f — +635 кДж, протекающей с поглощением тепла. В чистом виде такая реакция проходит при высоких температурах (— 1500 °С). Однако на практике в присутствии железа образуется силицид железа FeSi. Кремний выводится из сферы реакции. Равновесие реакции восстановления кремнезема сдвигается в правую сторону, т. е. в сторону образования кремния или силицидов, а сама реакция успешно протекает при значительно более низких температурах, например при 1050—1150 0C.
Для восстановления кремния необходимо увеличивать расход кокса, повышать температуру дутья, обогащать дутье кислородом, применять легковосстановимую железосодержащую шихту с тугоплавкой пустой породой, кремнезем которой равномерно распределен в массе оксидов железа. В доменной печи восстанавливается до 30 % кремния, остальное в виде SiO2 переходит в шлак. При производстве высококремнистых чугунов необходимо стремиться к получению шлака с пониженным содержанием извести, так как CaO связывает кремнезем в прочные соединения (силикаты), которые с трудом поддаются восстановлению. Обычно содержание кремния в передельных чугунах составляет 0,5—0,8 %, в литейных 0,7—3,8 %. При дефиците электрического ферросилиция в доменных печах иногда выплавляют бедный ферросилиций, содержащий 9—18 % кремния. Для этого в доменную печь приходится давать большое количество металлолома— до 450 кг на тонну сплава и значительно повышать долю кокса. В среднем на каждый процент кремния в чугуне расход кокса достигает 1000—1300 кг/т. И5 этих данных видно, что производство такого сплава в доменной печи малоэффективно.
Восстановление фосфора
Фосфор, находящийся в рудах в виде фосфорнокислого кальция Са3Р2O8, восстанавливается также раскаленным углеродом топлива в присутствии SiO2.
Кремний в доменном процессе
В доменной печи, кроме железа, восстанавливаются марганец, кремний, фосфор, а также мышьяк, титан, никель, медь, кобальт, ванадий, хром, цинк и другие элементы при их наличии в шихте. Не все элементы восстанавливаются в печи в одинаковой степени.
На рис. 56 приведено химическое сродство некоторых мeтaллoв и углерода к кислороду при разных температурах. Как известно, сродство металлов к кислороду с температурой убывает, а углерода к кислороду — возрастает. Точки пересечения линий металлов с линией углерода дают температуры, при которых сродство углерода равно сродству металла к кислороду. При температуре выше этих точек возможно непосредственное восстановление данного металла углеродом.
Из рис. 56 видно, что Сu, Ni образуют с кислородом менее прочные окислы, чем железо. Эти элементы в доменной печи восстанавливаются полностью. Наоборот, соединения хрома и марганца с кислородом прочнее, чем закись железа. Они в условиях доменной печи частично восстанавливаются, а некоторое количество Сr и Мn, находясь в виде закисей, растворяется в шкале (или возгоняется, окисляется в шахте до окислов и уносится с газом из печи). Также частично, но в меньшей степени восстанавливаются в доменной печи кремний и титан. Температура начала взаимодействия их окислов с твердым углеродом соответственно составляет 1790 и 1950°К. Окислы Аl2О3, СаО и МgO настолько прочны, что их металлы не присутствуют в чугуне: температуры восстановления Аl, Са и Mg твердым углеродом превышают температуры, достигаемые в доменной печи.

Ниже рассматриваются реакции восстановления элементов, присутствующих в чугуне.
В сырых материалах доменной плавки марганец может встречаться в виде двуокиси МnО2, окиси Мn2О3, закись — окиси Мn3O4 и закиси МnО. Эти окислы входят в состав минералов: пиролюзита, гаусманита, браунита, псиломелана и марганцевого шпата.
Химическое сродство первых трех окислов невелико, почему в условиях доменной печи окислы легко отдают часть кислорода, переходя в МnО. При этом МnО2 и Мn2О3 восстанавливаются до Мn3О4 по необратимым реакциям:

По обеим реакциям в равновесной фазе содержится углекислоты гораздо больше, чем в колошниковом газе.
Поэтому обе экзотермические реакции протекают в верхней части шахты печи, повышая температуру колошниковых газов (иногда до 700° и выше). От высокой температуры на колошнике коробятся металлические конструкции, изнашивается кладка вверху печи и наблюдается повышенный вынос с газами мелких частиц шихты. Во избежание этих реакций марганец стараются вводить в шихту в виде Мn3О4 или МnО. Одной из мер перевода высших окислов марганца в низшие является агломерация марганцевых руд: при высокой температуре агломерационного процесса МnО2 и Мn2О3 в атмосфере газовой фазы переходят в МnО.
Взаимодействие закись-окиси марганца с восстановителем проходит по реакции:
Эта реакция также протекает успешно при малых равновесных содержаниях окиси углерода (около 10% СО при температуре 700°) в ее смеси с углекислотой. Эти условия восстановления легче, чем для аналогичного ей окисла железа Fе3O4. Однако при высокой температуре верхней части шахты реакция получения МnО из Мn3О4 сопровождается взаимодействием СО2 с углеродом, отчего процесс восстановления в конечном счете протекает прямым путем:
Это невыгодно, так как уменьшается количество углерода, доходящего до горна.
Значительно труднее восстановить металлический марганец из закиси. Реакция
МnO + СO → Мn + СO2
может протекать, например, при 700° только при условии, что в газовой фазе содержание СО2 не превышает 0,01%. В доменной печи при 700° не может быть так мало СО2. Такое содержание СО2 возможно только при температурах выше 1000°, когда получаемая в результате восстановления СО2 полностью реагирует с углеродом. Таким образом, металлический марганец получается по реакциям:

Для восстановления закиси марганца твердым углеродом необходимы определенные температурные условия. Так, при температурах 600—700° процесс протекает даже в противоположном направлении
т. е. металлический марганец восстанавливает углерод из его окиси, как бы «горит» в атмосфере окиси углерода. Для направления реакции в сторону восстановления марганца требуются более высокие температуры.
При температурах выше 1100°, т. е. в области заплечиков и в горне, образуется карбид марганца Mn3C, углерод которого энергично восстанавливает Mn из MnO. Кроме того, образование Mn3C идет с выделением тепла, что облегчает течение эндотермической реакции восстановления марганца углеродом.
Двуокись марганца начинает восстанавливаться при 500° или при более низкой температуре. Примерно при этих же температурах отдает свой кислород окись марганца Mn2O3. Закись-окись марганца Mn3O4 — более прочный окисел и восстанавливается до МnО в интервале температур 570—1050°. Закись марганца MnO восстанавливается до металлического марганца твердым углеродом (древесного угля), начиная с 1100°; в присутствии железа восстановление начинается при 1030°, а в заметных количествах (от 15 до 73%) — при 1200—1400°. В вакууме процесс восстановления графитом начинается при температуре 850—900° и заканчивается при 1050°.
В условиях доменной печи не весь марганец полностью переходит в чугун. Окислы MnO2 и Mn2O3 восстанавливаются до Mn3O4 или до MnO. Соединение Mn3O4 обычно улетучивается (вернее возгоняется металлический марганец, а в верхних горизонтах он окисляется до Mn3O4 и в таком виде уходит из печи). Закись марганца частично восстанавливается до металлического марганца растворяющегося в чугуне; некоторое ее количество растворяется в шлаке.
Факторы, регулирующие количества восстановленного, переходящего в шлак и улетучивающегося марганца, будут рассмотрены ниже. Обычно в чугун переходит при плавке обычных марок 40—60% всего марганца; 5—10% уносится с газом, а остальное переходит в шлак.
Кремний может восстанавливаться только твердым углеродом в нижней части печи при высоких температурах. Даже при 1500° кремний восстанавливается в небольшом количестве, но в присутствии железа он восстанавливается при 1300°, причем реакция начинается уже при 1050°.
Железо облегчает восстановление кремния, видимо, потому, что образуются силициды Fe3Si; FeSi и FeSi2, которые распадаются на FeSi и Fe или FeSi и Si. Процесс их образования сопровождается выделением тепла, что облегчает восстановление. Восстановление кремния в присутствии железа облегчается еще и тем, что восстановленный кремний легко растворяется в железе.
В лабораторных условиях кремний восстанавливается из кварцевого песка твердым углеродом (кокса) при 1460°. В доменной печи благодаря летучести моноокиси кремния (SiO) восстановление облегчается, так как SiO интенсивно реагирует с восстановителем в парообразном состоянии. При восстановлении же из жидкой фазы углерод — продукт распада карбидов, будучи растворенным в чугуне, является тоже активным восстановителем. При температуре 1050° и выше уже присутствует большое количество восстановленного и обуглероженного железа, дающего этот активный углерод для восстановления кремния. Кроме того, углерод может быть получен из карбида кремния, образовавшегося после восстановления первых порций кремния.
Раньше предполагалось, что кремний получается из кремнезема непосредственно по реакции:
т. е. без образования промежуточных окислов.
Теперь доказано, что этот процесс, подобно восстановлению железа и марганца, идет ступенчато с возникновением промежуточного окисла — моноокиси кремния SiO. Так, при производстве ферросилиция в электропечах сумме всех компонентов в шлаке превышает 100%, если предположить, что весь кремний в них присутствует в виде SiO2; следовательно, приходится допустить, что часть Si находится в соединении SiO. Далее, белый дым, появляющийся над печами при выплавке ферросилиция, объясняется образованием моноокиси кремния, хотя ранее это относили к возгонке кремния или кремнекислоты. Кремний может быть восстановлен из кремнезема не только твердым углеродом, растворенным в металле. Восстановление может идти с помощью ранее полученного кремния. Поэтому возможны схемы восстановления

Роль кремния как восстановителя возрастает, когда в чугуне содержится мало углерода, т. е. при выплавке высококремнистых ферросплавов, но высококремнистый ферросилиций, содержащий более 15% Si, производится уже не в доменных, а в электропечах.
В таких случаях SiO из SiO2 получаются только с помощью кремния.
В доменном процессе получение SiO может происходить и с помощью углерода, растворенного в чугуне, и посредством ранее восстановленного кремния.
Фосфор находится в шихте в виде пятиокиси P2O5, соединенной с окислами железа или с известью в вивианит (FeO)3P2O5 и апатит (CaO)3P2O5. Фосфорнокальциевая и фосфорножелезистая соли являются более прочными соединениями, чем, например, карбонаты. Поэтому восстановление фосфора в печах происходит большей частью из соединений типа солей и реже — из свободной P2O5.
Фосфат железа начинает восстанавливаться водородом при 600°, а окисью углерода — при более высоких температурах, причем процесс интенсифицируется с ростом температуры. Особенно энергично идет восстановление водородом при 900—1000°, а окисью углерода — при 1000—1200°.
При восстановлении фосфора разрушается кристаллическая решетка фосфатов, вследствие чего из (FеO)3Р2O5 одновременно могут восстанавливаться и фосфор, и железо, почему процесс при умеренных температурах представляется таким образом:

(или аналогичным уравнением — с помощью водорода).
При температурах выше 950—1000° углекислота неустойчива в присутствии углерода, и суммарная реакция выражается уравнением:

При этом фосфид железа и фосфор растворяются в металле.
Процесс восстановления из фосфата кальция протекает иначе: реакция начинается только при 1100°, причем фосфор может восстанавливаться углеродом, окисью углерода и водородом. При 1300° получается только фосфор по реакции:

Обычно фосфорнокальциевая соль находится в железной руде, и ко времени протекания последней реакции уже имеется восстановленное железо, жадно поглощающее фосфор. Вследствие этого температура начала восстановления снижается.
Несмотря на отрицательный тепловой эффект, восстановление фосфора возможно и непрямым путем, так как в шихте содержится фосфора немного, и общее количество расходуемого тепла оказывается незначительным. По этой же причине прямое или непрямое восстановление фосфора не влияет на содержание СО2 в колошниковом газе и на расход кокса. Фосфор переходит в чугун практически весь.
Полное восстановление фосфора из Р2О5 объясняется сравнительно небольшим его сродством к кислороду, близким к железу, которое также практически восстановливается полностью. Этим же объясняется возможность восстановления фосфора непрямым путем, несмотря на эндотермичность процесса.
Сера кокса в большей части окисляется на фурмах кислородом дутья в SО2. Поднимаясь вверх с газами, SO2 восстанавливается твердым углеродом.
Сера легко соединяется с железом, давая сернистое железо FеS, растворяющееся в чугуне. Обычно небольшое количество серы остается в чугуне, значительная ее часть переходит в шлак, находясь в последнем в виде сульфидов CaS, MgS, MnS и FeS. Для получения указанных соединений требуется восстановить соответствующие количества Fe, Mn, Mg и Ca из их окислов. Следовательно, растворение серы в чугуне и в шлаке связано с восстановительными процессами.
В предыдущем были рассмотрены основные термодинамические условия восстановления железа, кремния, марганца, фосфора из свободных окислов. В доменной печи Si, Mn и P восстанавливаются большей частью из соединений их окислов с кремнеземом, глиноземом и др., т. е. из шлаков. Для комплексного изучения восстановления железа, марганца и кремния и путей борьбы с серой необходимо знать свойства шлаков. Поэтому подробно эти вопросы будут рассмотрены после изучения образования и свойств шлаков.
Все прочие элементы, присутствие которых возможно в металле, восстанавливаются в доменной плавке в зависимости от прочности их окислов и других условий. Так, медь, мышьяк, никель, цинк, свинец восстанавливаются в печи полностью, хром и ванадий — частично, титан — в небольших количествах; кальций, алюминий и магний вовсе не восстанавливаются.
Таким образом, окислы, характеризуемые малым химическим сродством металла к кислороду (Fe2O3, MnO2, Cu2O, NiO и др.) восстанавливаются в доменной печи до металлического состояния или до низшего окисла по необратимым реакциям при всех температурах доменного процесса. При умеренных температурах восстановление идет непрямым путем.
Наоборот прочные окислы (MnO, SiO2 и др.) не восстанавливаются окисью углерода при отсутствии твердого углерода, потому что газовая среда, содержащая самые незначительные количества CO2, уже способна окислять восстановленные металлы. Присутствие твердого углерода при высоких температурах обеспечивает частичное восстановление элементов из окислов этого типа прямым путем.
Наиболее прочные окислы Al2O3, MgO и CaO совсем не восстанавливаются в доменной печи.
Окислы, занимающие промежуточное положение, восстанавливаются окисью углерода, но при определенном соотношении CO2 и CO в газе. Металлы из таких окислов восстанавливаются частично непрямым, а частично прямым путем. Типичным примером такого процесса является восстановление Fe из FeO.
Кремний
Кремний поступает в доменную печь в виде диоксида кремния (SiO2), одного из основных компонентов пустой породы рудных материалов и золы кокса. Диоксид кремния может восстанавливаться только при высоких температурах (выше 1350 о С) в нижней части печи. В условиях доменной печи при высоких температурах восстановителемSiO2из пустой породы железорудных материалов может быть только углерод.
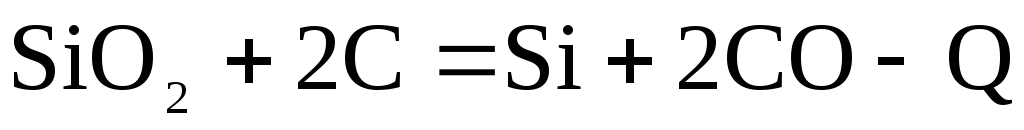
. (2.2‑28)
Так как реакция восстановления кремния экзотермическая, то чем выше температура, тем выше скорость реакции, т.е. количество восстановленного кремния в единицу времени. Следовательно, при высоких температурах в печи содержание кремния в чугуне будет выше.
Таким образом, основное условие восстановление кремния – это высокая температура. Влияние температуры на степень восстановления кремния столь велико, что содержание кремния в чугуне используется доменщиками как важнейший показатель нагрева печи. Поэтому доменщики внимательно следят за изменением содержания кремния в выпускаемом чугуне, определяя его не только путем химического анализа, но и по виду излома пробы и виду текущего по желобу чугуна. Нагрев печи можно изменить, изменив приход тепла в печь. Основным средством для этого является изменение удельного расхода топлива.
Так как процесс восстановления кремния идет с увеличением объема газовой фазы, увеличение давления в доменной печи будет затруднять восстановление кремния. Опыт работы современных доменных печей на повышенном давлении подтверждает этот факт. Содержание кремния в передельном чугуне при нормальном температурном режиме составляет до 0,01%.
SiO2– кислотный оксид и в основных шлаках он связывается оксидом кальция в силикаты кальция (CaSiO3). Восстановления кремния из этого соединения требует еще больших затрат тепла и, следовательно еще более высоких температур:
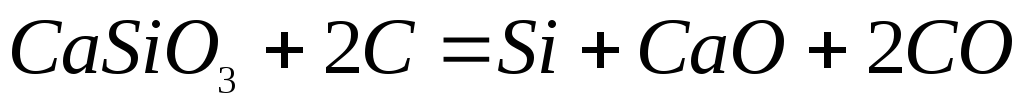
– 26 000 кДж/кг Si. (2.2‑29)
Поэтому, чем ниже основность шлаков (CaO/SiO2), тем лучше условия восстановления кремния.
Количество шлака также влияние на степень восстановления кремния. Чем меньше шлака, тем ниже затраты тепла на производство чугуна и тем легче повысить температуру в печи. Поэтому условием увеличения степени восстановления кремния является работа с меньшим выходом шлака (использование богатых железорудных материалов).
Таким образом, для повышения степени восстановления кремния необходимы высокие температуры и низкий выход кислого шлака.
Фактическое содержание кремния в чугуне далеко от равновесного. Поэтому можно считать, что содержание кремния в чугуне зависит от кинетики процесса, т.е. времени пребывания расплава на коксовой насадке.
Степень восстановления кремния в доменных печах при выплавке передельных чугунов составляет всего 3…8%. При выплавке литейных чугунов температуры в печи создаются более высокими и степень восстановления кремния поднимается до 15…25% и только при выплавке ферросилиция, когда создаются наиболее благоприятные условия для восстановления кремния, она достигает 35…50%.
Фосфор в доменные печи попадает, главным образом, с рудными материалами в виде ортофосфата кальция Ca3(PO4)2и подобных ему соединений. Несмотря на то что, оксид фосфора очень прочное соединение (восстановление его возможно только при высоких температурах в области прямого восстановления), в доменной печи фосфор полностью восстанавливается и переходит в чугун.
Полному восстановлению фосфора способствует ряд обстоятельств:
Фосфора в доменные печи попадает сравнительно мало (но не с точки зрения получения качественного чугуна, а с точки зрения его относительного количества).
В пустой породе рудных материалов и золе кокса имеется достаточно двуокиси кремния, которая вытесняет пятиокись фосфора из ее соединений с основными окислами (P2O5 — кислый окисел).
Восстановленный фосфор образует фосфиды железа (FeP) и таким образом удаляется из системы реагирующих компонентов. Растворение фосфора в железе сдвигает равновесие в сторону образования фосфора.
Вследствие указанных причин процесс восстановления фосфора идет практически необратимо:
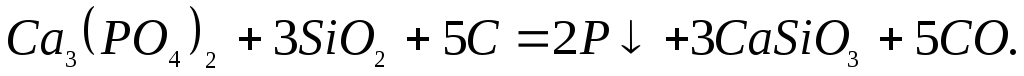
2.2‑30)
Таким образом, учитывая, что фосфор полностью переходит в чугун, единственным средством борьбы с фосфором при производстве чугуна является использование чистых по фосфору шихтовых материалов.
Сера в доменную печь вносится шихтовыми материалами и топливом, вдуваемым через воздушные фурмы с дутьем. Наибольшее количество серы вносит кокс. На его долю приходится не менее 50 % серы, поступающей в печь. Как правило, эта доля достигает 65 % и более, а в ряде случаев — 90 %.

В коксе сера, в основном (на 80 %), является органической, т.е. находится в виде органических соединений, входящих в состав горючей массы кокса. Остальная сера — это сера, входящая в состав золы кокса, является сульфидной серой, связанной с железом в .
В железорудных материалах сера находится в виде:
сульфидов: пирита (), пирротина () и др. — в магнитных железняках;
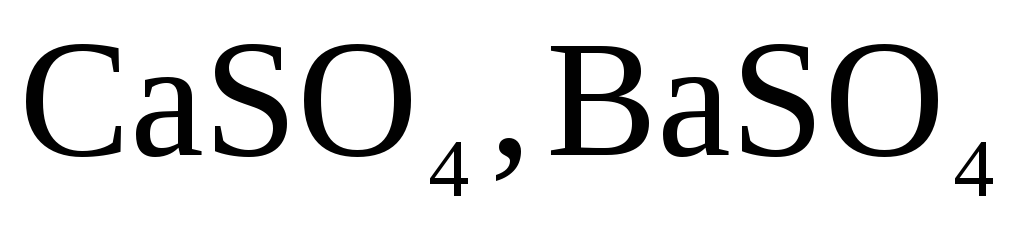
сульфатов: и др. – окисленных рудах, агломератах и окатышах.
Вдуваемое с дутьем топливо также может содержать серу – угольная пыль и мазут. Сера в них содержится в виде органических соединений.
Органическая сера кокса в основной своей массе доходит до фурм и вместе с углеродом сгорает по реакции
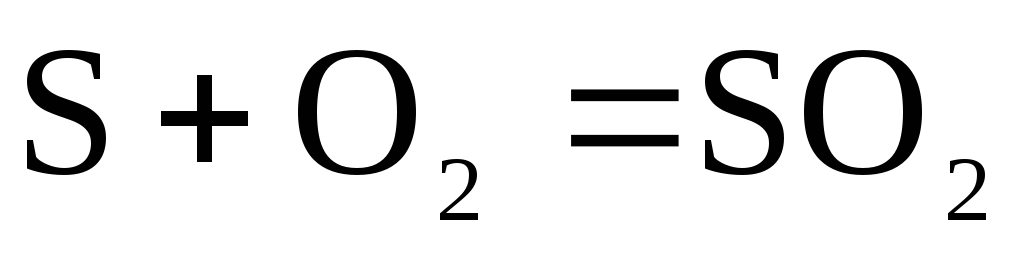
. (2.2‑31)
Поднимаясь с газами через слой раскаленных материалов, в заплечиках и распаре печи сернистый газ взаимодействует с и углеродом с образованием сульфидов железаи кальция по реакциям
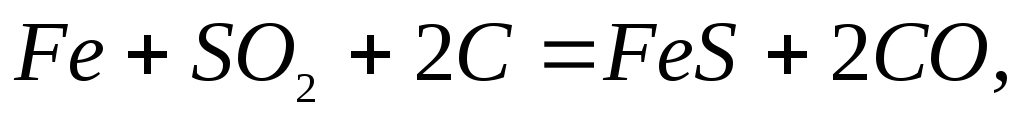
(2.2‑32)
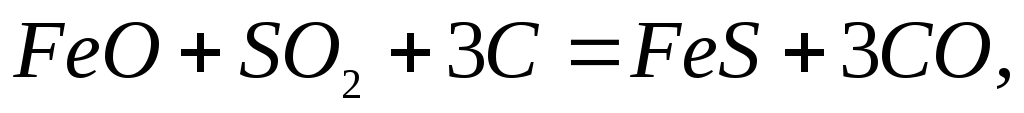
(2.2‑33)
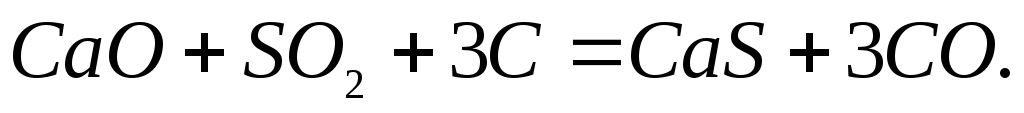
(2.2‑34)
В этих процессах сера восстанавливается из до элементной серы и взаимодействует собразуя соответствующие сульфиды.
Попавшие в доменную печь сульфаты при высоких температурах будут восстанавливаться углеродом по реакции
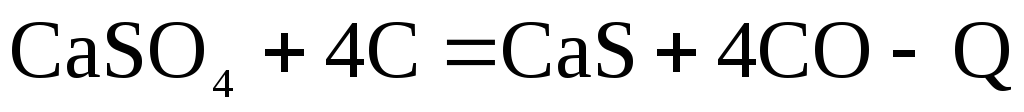
. (2.2‑35)
Таким образом, в результате описанных процессов сера будет находиться либо в виде , хорошо растворимом в чугуне, либо в виде, растворимом в шлаке и не растворимом в чугуне.
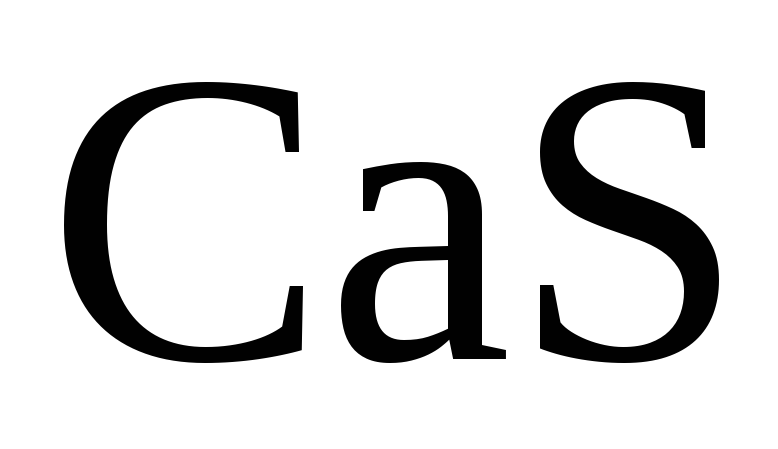
Чтобы получить чистый по сере металл, необходимо как можно больше серы перевести в , т.е. в шлак. Это возможно в результате следующих реакций:
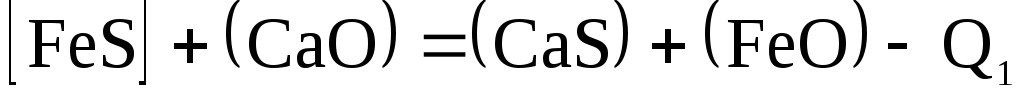
(2.2‑36)
Процесс удаления серы из чугуна протекает при высоких температурах. Поскольку атмосфера в доменной печи восстановительная и имеется достаточное количество углерода, то FeO восстанавливается углеродом:
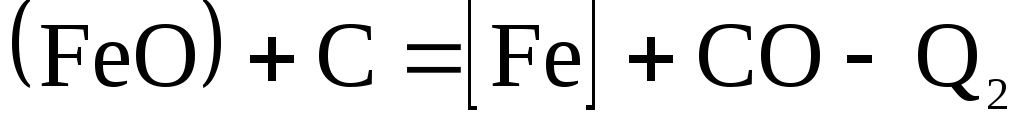
(2.2‑37)
Это обстоятельство является характерной особенностью десульфурации в доменных печах, которая может быть представлена суммарной реакцией:
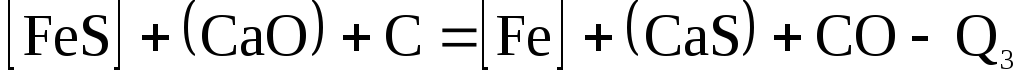
(2.2‑38)
Образующийся при этом, сульфид кальция не растворяется в металле и переходит в шлак.
Как видно из уравнений, вещества, участвующие в процессе десульфурации находятся либо в чугуне (FeS, Fe, C), либо в шлаке (CaO, CaS).
Поэтому процесс десульфурации может протекать на границе их раздела. Наиболее благоприятные условия для его развития в горне печи, когда капли чугуна проходят через слой шлака.
Условия равновесия рассматриваемого процесса выражаются константой равновесия, которая является функцией только температуры:
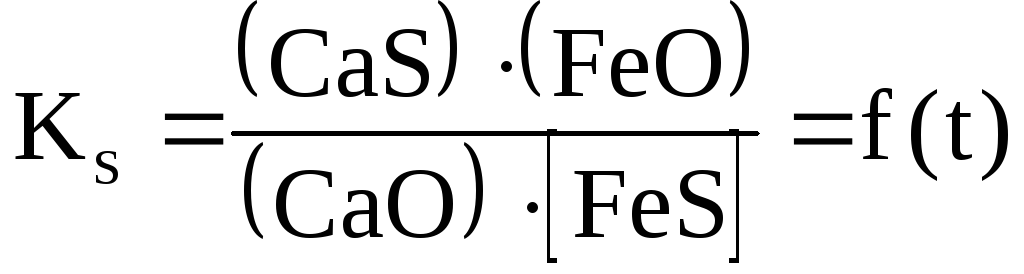
. (2.2‑39)
Поскольку содержание серы в шлаке пропорционально содержанию в а содержание серы в чугуне пропорционально содержаниюв чугуне, то константа равновесия может быть записана в виде:
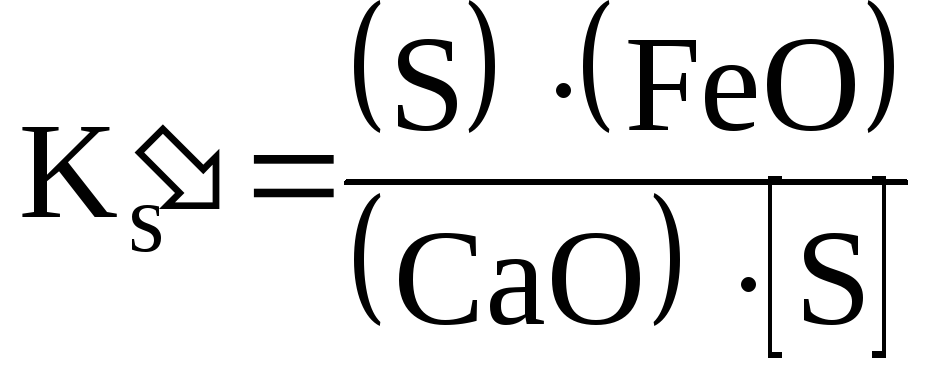
. (2.2‑40)
Из этих уравнений следует, что для снижения содержания серы в чугуне надо увеличивать концентрациюв шлаке и уменьшать величиныи
Известно, что константа равновесия реакции десульфурации является функцией температуры. Поскольку реакции десульфурации идут с поглощением тепла, то с повышением температуры, согласно принципу Ле-Шателье, ее равновесие сдвигается вправо, т.е. в сторону увеличения концентрации . Поэтому, чем выше температура, тем выше значениеи, следовательно, содержание серы в металле. Практический интерес для нас представляет содержание серы в чугуне. Уравнение, связывающее содержание серы в чугуне с параметрами шихты, шлака и константой равновесия можно получить на основе баланса серы, который записывается следующим образом:
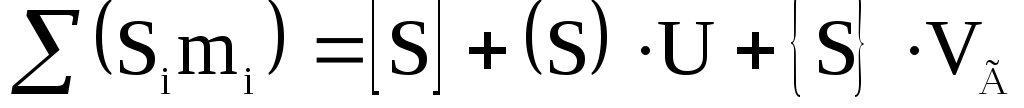
, (2.2‑41)
где – соответственно, содержание серы вi-ом материале, в чугуне, шлаке и газе;– удельный расходi-го материала;– удельный выход шлака;– удельный выход газа.
Основная часть серы распределяется между чугуном и шлаком. Отношение концентраций серы в шлаке и чугуненазывается коэффициентом распределения серы
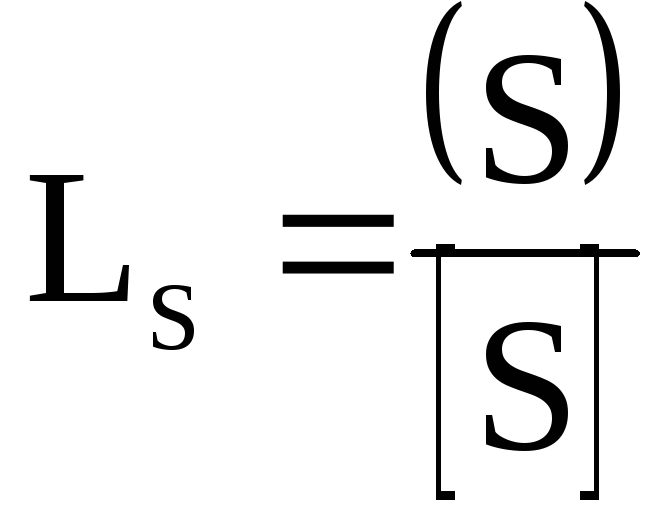
. (2.2‑42)
Коэффициент распределения серы может быть выражен следующим образом:
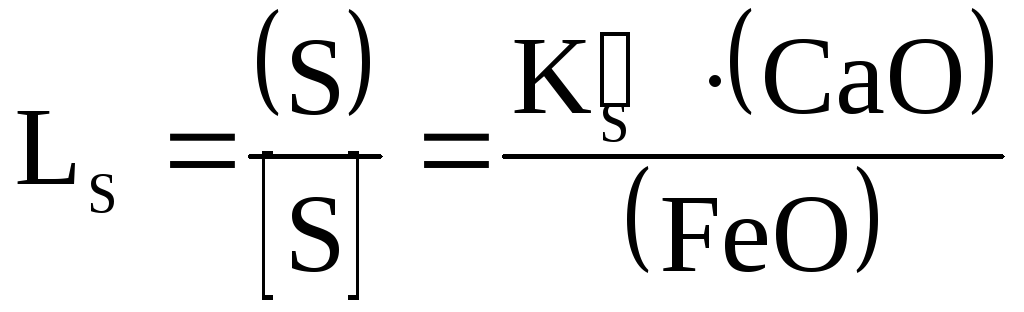
. (2.2‑43)
Как и константа равновесия , коэффициент распределения серы является функцией температуры и основности шлака. Выразив содержание серы в шлаке черезполучим

Подставив это выражение в правую часть балансового уравнения вместо , будем иметь:
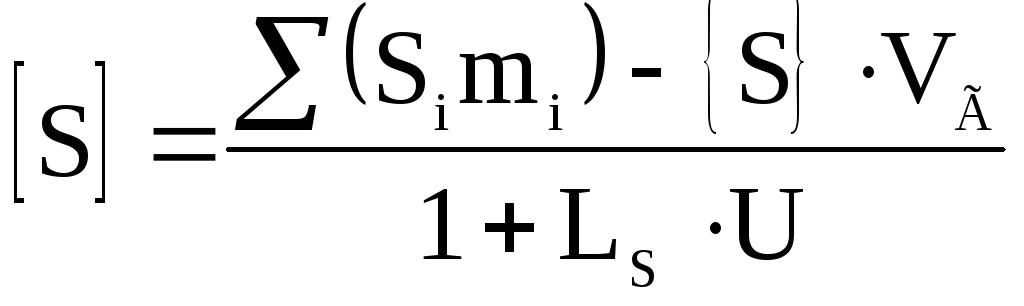
. (2.2‑44)
Поскольку значение с ростом температуры и основности шлака возрастает, то из этого уравнения вытекает, что для максимального удаления серы из металла в шлак необходимо повышение температуры и основности шлака, повышение выхода шлака и снижение серы в шихтовых материалах.
Из рассмотренного видно, что удаление серы связано с увеличением удельного расхода топлива, а это в свою очередь приводит к снижению производительности печи.
В связи с этим представляет интерес внедоменная десульфурация чугуна. Она позволяет вывести процесс десульфурации из доменной печи, работать при малых выходах кислого шлака и нормальных температурах в печи, и, следовательно, иметь низкий удельный расход кокса и высокую производительность печи.
Существует несколько способов внедоменной десульфурации чугуна, которые отличаются реагентами, используемыми для этой цели, способом их присадки в чугун, конструкцией устройств для ввода присадок и т.д. Основной технологией десульфурации чугуна является вдувание реагентов (известь, карбид кальция, металлический магний) в чугуновозный ковш азотом.
Никель, медь, кобальтполностью переходят в чугун, и их содержание в чугуне зависит от количества этих металлов в шихте.
Хром, ванадий титанв доменных печах восстанавливаются и переходят в чугун частично (Cr на 80-90%, V — 70-90%, Ti — 3-5%), а не восстановленная часть их окислов переходит в шлак.
Цинк, полностью восстанавливается, испаряется и, попадая с газами в верхнюю часть печи и в газоотводы, конденсируется на восстановленном железе. Это явление затрудняет косвенное восстановление оксидов железа, что ведет к перерасходу кокса. Опускаясь вместе с рудными материалами, цинк снова испаряется. В доменной печи цинк накапливается и образует зону циркуляции. Часть цинка в виде мелких частиц цинкита газами проникает в поры и трещины огнеупорной кладки и там конденсируется, а также уносится из печи газами и осаждается в системе газоочистки. Накопившиеся в порах, швах и трещинах кладки печи, цинк и цинкит могут вызвать в ней напряжения. Кроме того на стенках печи могут образовываться так называемые настыли. На качество чугуна цинк никакого влияния не оказывает.
Восстановленный свинецбыстро стекает в горн и, поскольку он более плотный и не растворяется в чугуне, то скапливается на лещади печи самостоятельным слоем. Будучи сильно перегретым, он, имея малую вязкость и высокую плотность, легко проникает в поры и швы огнеупорной кладки и разрушает ее.
Источник https://infopedia.su/15×2069.html
Источник https://metal-archive.ru/domennyy-process/2101-vosstanovlenie-kremniya-marganca-fosfora-i-prochih-elementov.html
Источник https://studfile.net/preview/1865388/page:7/