Тяжелых металлов в растениях
27-09-2017, 19:08
Химический состав растений отражает элементный состав почвенной среды. Однако на эту общую закономерность оказывают влияние многие факторы. Поэтому содержание тяжелых металлов в растениях очень изменчиво и на не загрязненных почвах колеблется в широких интервалах. В условиях химических стрессов, вызванных избытком элементов, растения в ходе эволюции выработали механизмы, приводящие к устойчивости к нарушениям химического баланса в окружающей среде.
Главный путь поступления металлов в растения — это абсорбция корнями. Поэтому почвенная среда — основной источник элементов для растений, корневая система которых может поглощать тяжелые металлы активно (метаболически) и пассивно (неметаболически). В большинстве случаев скорость поглощения элементов положительно коррелирует с содержанием их доступных форм. На эту главную закономерность оказывают влияние ряд факторов: 1) реакция среды, 2) концентрация кальция, магния и других ионов, 3) такие свойства почвенной среды как температура, аэрация, окислительно-восстановительный потенциал, 4) вид растений и стадия его развития. Поэтому зависимость между степенью загрязнения почвы тяжелыми металлами и интенсивностью их поступления в растения является сложной и не носит функционального характера. Объясняется это тем. что не все растения обладают одинаковой способностью накапливать тяжелые металлы. Это свойство связано с наличием у растений в разной степени выраженности различных физиолого-биохимических защитных механизмов, препятствующих поступлению токсичных элементов.
Несмотря на существенную изменчивость в способности различных растений к накоплению тяжелых металлов, биоаккумуляция элементов имеет определенную тенденцию. Так, например, по степени накопления выделяется несколько групп элементов:
1. Cd, Cs, Rb — поглощаются легко.
2. Zn, Mo, Cu, Pb, Ag, As, Co — средняя степень поглощения.
3 Mn, Ni, Li, Cr, Be, Sb — слабо поглощаются.
4 Se, Fe, Zn, Ba, Te — трудно доступны растениям.
Тяжелые металлы могут поступать в растения и некорневым путем из воздушных потоков. На практике широко применяется опрыскивание растений растворами микроэлементов железа, меди, марганца, молибдена и других. Поступление элементов в растения через листья или фолиарное поглощение происходит, главным образом, путем неметаболического проникновения через кутикулу. Поглощенные листьями металлы могут переноситься в другие растительные ткани, в частности в корни, в которых могут находиться длительное время в форме запаса. При переносе катионов в растениях наиболее важную роль выполняют хелатообразующие лиганды.
Между концентраций металлов в почвенных растворах и их поглощением корнями растений, как правило, существует прямая линейная зависимость. Это положение свидетельствует о том. что не запас тяжелых металлов в почве, а их воднорастворимые или подвижные формы определяют доступность элементов для растений. На этом принципиальном положении основана разработка методов определения подвижных, или доступных для растений элементов путем кислотной экстракции или применения специфических ее комплексообразователей.
Несмотря на положительную функциональную зависимость между концентрацией тяжелых металлов в почвенном растворе и поглощением их растениями, количественное выражение этой закономерности для разных металлов существенно различается. Так. при увеличении концентрации элементов в растворе содержание свинца в растениях возрастает в несколько раз медленнее по сравнению с кадмием. По скорости накопления в растениях с ростом концентрации элемента в растворе тяжелые металлы составляют следующий ряд: Cd>Zn>Cu>Pb. Наши экспериментальные данные (рис.6, 7, 8), характеризуют зависимость поступления Cd, Zn и Pb в растения при увеличении их содержания в почве и изменении ее кислотности. Увеличение концентрации в почве кадмия, цинка и свинца сопровождаюсь возрастанием их содержания в корнеплодах свеклы. Однако интенсивность этого процесса сильно зависела от уровня реакции среды в почве. Изменение pH почвы с 4,5 до 7 в 5-10 раз снижаю содержание кадмия, цинка и свинца в растениях при самом высоком их содержании в почве. При pH 7 и содержании в почве 500 мг/кг цинка получены корнеплоды свеклы, соответствующие санитарно-гигиеническим нормам в отношении этого металла. При pH почвы 4,5 и той же концентрации этого элемента в почве содержание цинка в корнеплодах превысило ПДК в 4,6 раза. В условиях слабощелочной реакции среды содержание свинца в корнеплодах свеклы было ниже ПДК даже при концентрации этого элемента в почве, равной 500 мг/кг. Приведенные данные опытов свидетельствуют о том, что действие реакции среды в почве может быть более сильным фактором. чем концентрация тяжелых металлов.
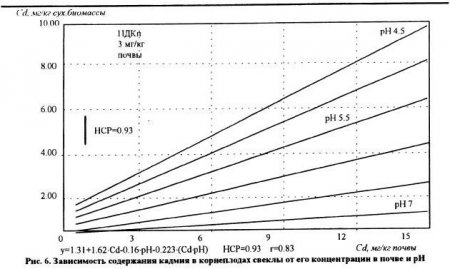
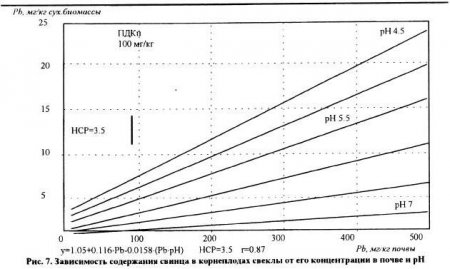
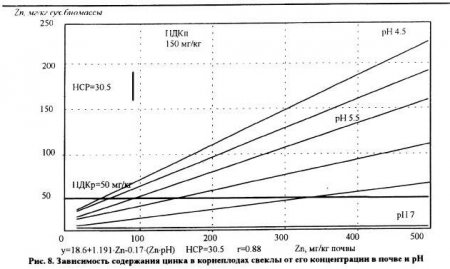
В настоящее время установлено, что фитотоксичность тяжелых металлов, устойчивость к ним растений и содержание этих элементов в растениях зависят от многих условий. О механизмах устойчивости различных культур к повышенным концентрациям тяжелых металлов пока накоплено мало сведений. Известно. что есть растения, способные концентрировать отдельные металлы без видимых признаков угнетения. На фитотоксичность металлов большое влияние оказывают такие свойства почвы как уровень реакции среды, емкость катионного обмена, содержание органического вещества и другие. Наиболее активное влияние на подвижность металлов в почвах и их усвоение корневыми системами растений оказывает кислотность почвы. Органическое вещество почвы также играет большую роль в снижении доступности тяжелых металлов для растений. Однако при этом многое зависит от свойств конкретных металлов. Так, органическим веществом активнее закрепляются медь и свинец и значительно слабее цинк и кадмий. Влияние свойств почвы и удобрений при разной концентрации металлов на содержание их в растениях схематически приведено на рис. 9 (К. Рэуце, Кырстя. 1986).
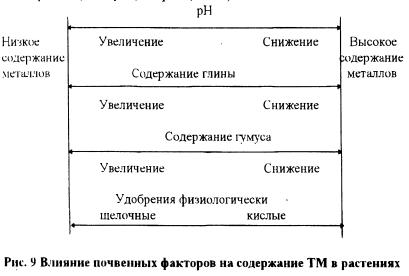
В настоящее время накоплено к сожалению недостаточно экспериментальных данных по содержанию тяжелых металлов в растениях.
Содержание Cu в растениях, характерное для незагрязненных районов, колеблется от 1 до 30 мг/кг сухой массы, а в золе различных видов растений — от 5 до 1500 мг/кг. Концентрация меди, в растениях, превышающая 20 мг/кг сухой массы, условно считается пороговой, определяющей области нормального и избыточного содержания меди в растениях. Содержание цинка в некоторых культурах колеблется в следующих интервалах (мг/кг сухого вещества): в зерне пшеницы от 22 до 33, травах от 12 до 41. в клевере от 24 до 45, листьях салата достигает более 70 мг. в яблоках в пределах 1-1,5. Загрязнение окружающей среды цинком увеличивает концентрацию этого элемента в растениях, которая может достигать десятых долей процента.
Наибольшее содержание кадмия зафиксировано в листовых овощах. В условиях незагрязненных почв наибольшая его концентрация характерна для листьев шпината и салата-латука (0.6-0.7 мг/кг на сухую массу, около 3,0 мг/кг в золе). Фоновое содержание кадмия в различных растениях составляет следующие величины (мг/кг сырой массы): в зерне 0,01-1,007; листьях капусты 0,02-0,05; салате и шпинате 0,11-0,42; моркови (корнеплоды) 0,05-0,15; луке (луковицы) — 0,01-0,05; картофеле (клубни) 0,001-0,08; томатах (плоды) 0,02-0,11; яблоках 0,003-0,03. Поскольку растения легко извлекают Cd из почвенных и воздушных источников, то его концентрация в растительной продукции в загрязненных районах повышается. В этих районах наибольшая концентрация кадмия обнаруживается в корнях и листьях (в зерне его содержание чаще остается низким). Содержание кадмия в пищевых и кормовых растениях должно контролироваться особенно тщательно, так как кадмий в питании человека и животных представляет кумулятивный яд.
Содержание свинца в пищевых продуктах в незагрязненных областях составляет 0,05-3,0 мг/кг сухой массы. Фоновые уровни содержания свинца в кормовых растениях составляет в среднем (мг/кг сухой массы): в травах 2,1 (колебания возможны от 1 до 9). в клевере 2,5 (колебания от 1 до 8). В загрязненных районах растения могут поглощать свинец как из почвы, так и из воздуха, что приводит к аномальному его накоплению особенно в листовых овощах. Содержание свинца в травах может достигать 63-232 мг. в клубнях картофеля 10-20 мг, в моркови 27-57 мг на кг сухой массы.
По способности поглощать соединения ртути растения существенно различаются. Содержание ртути в зерне обычно составляет 3-8 мкг, в овощах 2,6-86 мкг на кг сухой массы, а во фруктах от 0,6 до 70 мкг/кг влажной массы. Использование ртутных препаратов при обработке семян может приводить к увеличению содержания ртути в сухой массе растения до 170 мкг/кг.
По данным многих авторов содержание ртути в растениях резко различалось (например, в зерне разных стран от 0,2 до 82 мкг/кг сухой массы).
Наиболее высокое содержание хрома отмечено в корнях растений, а наименьшее — в зерне. Данных о его содержании в растениях недостаточно. Концентрация Cr в растительном материале обычно составляет 0,02-0,2 мг/кг сухой массы, однако отмечены очень резкие колебания в содержании этого элемента в растительной продукции. При высоком содержании хрома в почве проявляется его токсическое действие на растения. При этом увеличивается не только содержание хрома в растениях, но и снижается содержание основных питательных элементов: калия, фосфора, железа и магния в них.
Результаты длительных опытов НИИОХ свидетельствуют о том, что между содержанием в овощах сухих веществ и тяжелых металлов существует прямая зависимость. По способности накапливать тяжелые металлы основные овощные культуры в порядке возрастания располагаются в следующей последовательности: капуста — морковь — столовая свекла.
В среднем за 3 года на незагрязненной тяжелыми металлами почве содержание металлов в кочанах капусты (мг/кг сырой массы) составило: Cu 0,29-0,36; Zn 1,68-2,66; Mo 0,016-0,25; Co 0,003-0,004; Pb 0,01-0,03; Cd 0,003-0,009. При внесении микроудобрений (Co, Cu, Mo и Zn) их содержание в кочанах возрастало для меди и цинка на 20-40%, а для кобальта и молибдена в 2-3 раза. Содержание металлов в корнеплодах моркови составило (мг/кг сырой массы): Cu 0,56-0,82: Zn 2,75-3,54; Mo 0,014-0,035: Co 0,003-0,007; Pb 0,03-0,07; Cd 0,003-0.035. В корнеплодах свеклы столовой среднее содержание металлов составляло (мг/кг сырой массы): Cu 0,7-1,48; Zn 3,53-4,86; Mo 0,028-0,038: Co 0,009-0,013; Pb 0,04-0,18; Cd 0,02-0,04.
Концентрация металлов в растениях может сильно меняться в зависимости от многих условий. В таблице 64 приведены данные о содержании элементов в зрелых тканях листьев по обобщенным материалам для многих видов растений (А. Кабата-Пендиас, X. Пендиас, 1989) за исключением очень чувствительных или сильно устойчивых видов.
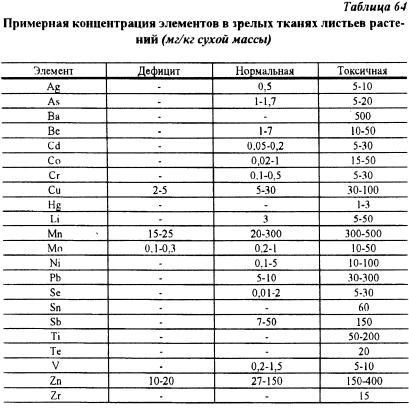
Авторы, приведенных в таблице обобщенных материалов, подчеркивают, что указанные интервалы концентраций микроэлементов имеют очень приближенное значение для конкретных частных систем: почва — растение. Точную границу между нормативным или достаточным и избыточным количеством тяжелых металлов в растениях провести трудно, так как граница между безвредным и токсичным действием на метаболизм растений часто бывает очень близкой.
Пределы колебаний нормальных концентраций тяжелых металлов в растениях (табл. 65), приведенные В.Г. Минеевым, 1990 г., на основании данных N El — Bascam и Thorman. свидетельствуют о том, что для большинства элементов их количественные параметры в растениях могут изменяться в 10 и более раз.
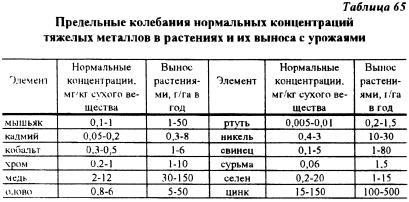
На загрязненных тяжелыми металлами почвах содержание тяжелых металлов в растениях может возрастать в несколько раз. особенно в случаях, когда фоновое содержание этих элементов в результате антропогенных нагрузок многократно увеличивается. Это положение хорошо иллюстрируют данные Thornton (в монографии В.Б. Ильина, 1991) о содержании тяжелых металлов в овощах на почвах различной степени загрязненности в Англии (табл. 66).
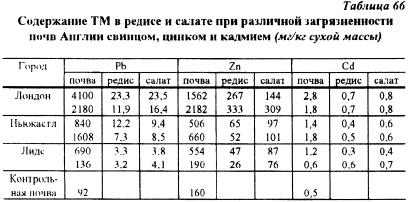
По данным В.Б. Ильина с соавторами (1985) на расстоянии 1 км от металлургических комбинатов содержание цинка свинца и кадмия в картофеле, и особенно овощных культурах, сильно увеличивалось (табл 67).
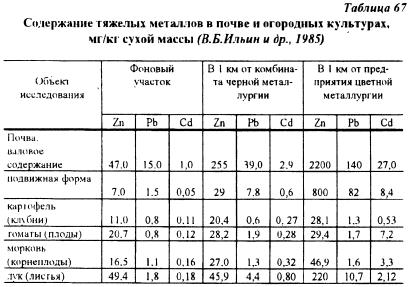
Например, содержание кадмия в растениях, выращиваемых в зоне предприятия цветной металлургии, возросло в картофеле в 4,8 раза, в томатах — в 60 раз, моркови — в 21 раз и луке — в 12 раз. Следует отметить, что на загрязненной в очень сильной степени кадмием почве содержание этого металла в клубнях картофеля было намного ниже, чем в овощных культурах. Эти данные свидетельствуют о больших потенциальных возможностях картофеля при размещении этой культуры на загрязненных почвах с целью получения пригодной для использования в пищу продукции.
Видовые особенности культур определяют распределение металлов по органам. Корни растений до определенного предела обеспечивают защиту надземных органов. Если, несмотря на защитную функцию корней, токсикант проникает в стебель и листья, то растение способно ограничить его поступление в репродуктивные органы. В таблице 68 приведено содержание меди и никеля в различных растениях в зависимости от концентрации этих металлов в почвах (Евдокимова, Мозговая, 1988; Соборникова, Фомина и др. 1988).
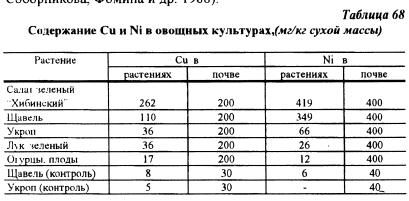
Показано, что при одинаковом содержании в почве меди и никеля их концентрация в различных растениях изменялась в 2-35 раз. Наибольшим содержанием меди и никеля отличались салат и щавель.
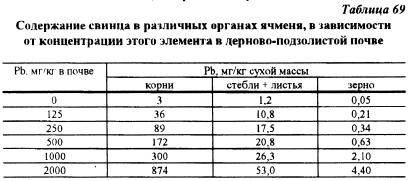
По мере увеличения содержания тяжелых металлов в почве до очень высокого уровня концентрация их в различных органах увеличивается. Ho при этом сохраняется соотношение между содержанием тяжелых металлов в корнях, стеблях, листьях и репродуктивных органах. Это положение можно проиллюстрировать результатами исследований Н.А. Черных (1988) с ячменем. выращиваемом на почве, в которую был внесен свинец в возрастающих дозах от 125 до 2000 мг/кг (табл. 69). Приведенные материалы свидетельствуют о том, что несмотря на резкое (почти в 300 раз) увеличение содержания свинца в корнях ячменя. концентрация этого элемента в стеблях, листьях и зерне также возросла, но в меньшем количественном выражении: в стеблях и листьях — в 44, в зерне — в 88 раз.
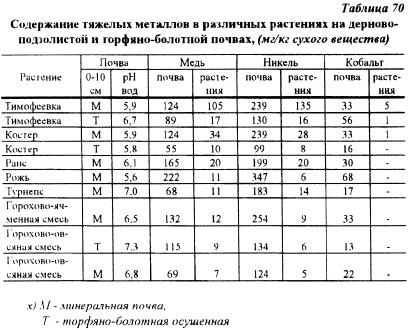
При прогнозировании поступления TM в растения следует принимать во внимание также различие в содержании металлов в культурах, выращенных на разных типах почв. Так, наименьшее поступление меди в растения наблюдается на торфянистых почвах, затем в возрастающем порядке идут черноземы, сероземы. известкованные дерново-подзолистые и, наконец, кислые дерново-подзолистые почвы. В таблице 70 приведены данные о содержании в различных растениях меди, никеля и кобальта, выращенных на минеральной и торфяно-болотной почвах. Растения существенно различались по содержанию изучаемых элементов. Ho типовые различия почв оказали большее влияние на содержание тяжелых металлов в растениях, чем их видовые особенности. Содержание меди, никеля и кобальта в растениях, выращенных на торфяно-болотной почве, было значительно меньше, чем у растений на минеральной почве (Г.А. Евдокимова, H.Г. Мозговая, 1988).
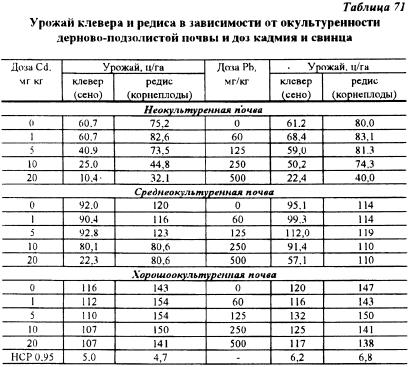
В условиях микрополевых опытов ЦОС ВИУА (Московская область) исследовано влияние различных концентраций тяжелых металлов (Pb, Cd, Cu и Zn) на урожай различных сельскохозяйственных культур, его качество. В этих опытах выявлены закономерности поступления тяжелых металлов в растения в зависимости от степени плодородия тяжело-суглинистой дерново-подзолистой почвы. Результаты исследований показали, что по мере увеличения дозы тяжелых металлов, вносимых в почву, возросло их содержание в растениях, приводящее к падению урожаев культур, снижению качества получаемой продукции и. в конечном счете, к гибели растений. Однако, токсичное действие металлов проявлялось неоднозначно на разных по окультуренности почвах. Наибольший токсический эффект обнаружен на кислой дерново-подзолистой почве. Окультуривание почвы привело к снижению токсичности всех изучаемых металлов. Отмечена большая токсичность меди и цинка по сравнению со свинцом: при дозе Cu — 60 мг/кг и Zn — 250 мг/кг растения клевера и редиса погибали, тогда как их гибель в опыте со свинцом не происходила даже при дозе 500 мг/кг на дерново-подзолистой неокультуренной почве (табл. 71, 72).
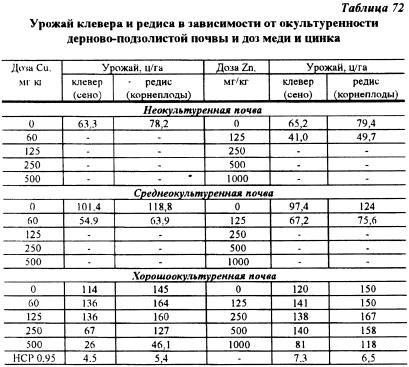
Увеличение доз кадмия, свинца, меди и цинка привело к возрастанию содержания этих элементов в клевере и редисе (табл. 73). Окультуренность почвы оказала слабое влияние на уменьшение поступления тяжелых металлов в растения клевера и редиса. Главным фактором загрязнения растительной продукции были дозы тяжелых металлов. Следовательно, буферная способность почвы ограничивать поступление тяжелых металлов может лишь в определенных пределах.
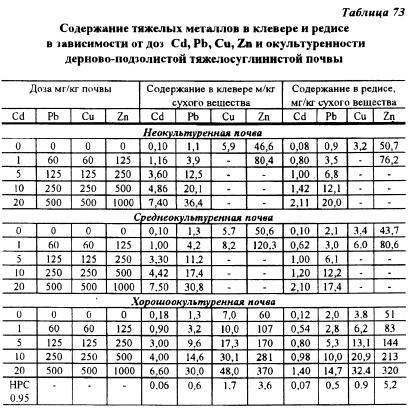
В условиях микрополевых опытов на ЦОС ВИУА изучалось влияние различных приемов, влияющих на фитотоксичность кадмия и накопление этого элемента в растениях. Результаты проведенных исследований показали, что наибольшим детоксикационным действием обладают известкование и внесение навоза, а также их сочетание. Действие торфа и цеолита проявилось намного слабее. При сочетании извести, навоза, торфа и цеолита даже при очень высоком содержании в почве кадмия (50 мг/кг) урожай зерна ячменя был выше, чем на почве без внесения кадмия, а сена клевера на этом уровне (табл. 74).
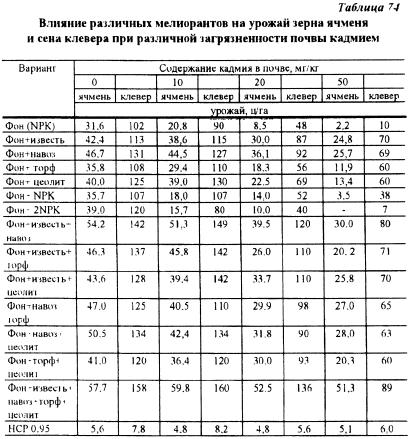
Среди отдельных факторов наибольшее влияние на снижение поступления в растения кадмия оказало известкование. Сочетание всех приемов: известкования и внесения в почву навоза, торфа и цеолита дало наибольший эффект по снижению содержания кадмия в зерне ячменя и сене клевера. Удвоение дозы минеральных удобрений не оказало существенного влияния на урожай, что. по-видимому, было причиной отсутствия их действия на концентрацию кадмия в растениях (табл. 75).
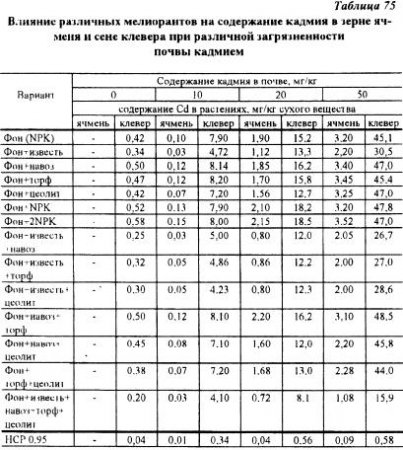
Исследования, проведенные в данном опыте, показали, что, накапливаясь в растениях, тяжелые металлы оказывают сильное влияние на содержание питательных элементов (табл. 76, 77). При этом происходит сильное изменение соотношения питательных веществ. Так. например, увеличение доз кадмия и свинца привело к существенному увеличению содержания азота в клевере на слабоокультуренной почве. На окультуренной почве аналогичное явление наблюдалось также при увеличении доз меди и цинка, вносимых в почву. Одновременно по мере увеличения доз тяжелых металлов снижалось содержание в растениях клевера фосфора. Причем содержание фосфора в растениях снижалось очень резко, в большинстве случаев почти в 2 раза. Следует также отметить факт резкого снижения содержания кальция в растениях по мере увеличения доз тяжелых металлов. Например, на хорошоокультуренной почве увеличение дозы кадмия с 1 до 20 мг/кг почвы привело к уменьшению содержания кальция в растениях клевера с 0,56 до 0,19%. то есть в 3 раза. Содержание магния и калия в сене клевера от доз тяжелых металлов зависело в меньшей степени.
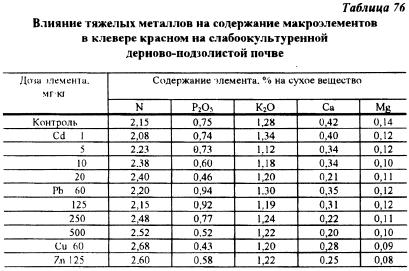
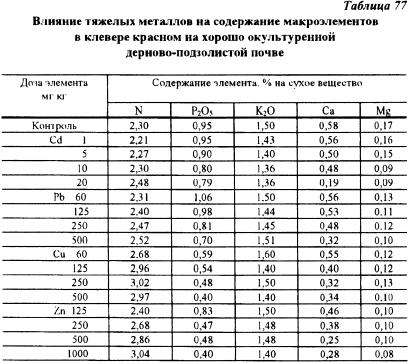
Тяжелые металлы оказывали и более глубокое влияние на химический состав растений. Так, отношение Pорг : Рмин снижалось с 3,05 до 2,20 на максимальных дозах тяжелых металлов в опыте с хорошоокультуренной почвой и с 2,6 до 1,6 — на слабоокультуренной почве. В растениях клевера под влиянием тяжелых металлов увеличивалось содержание нитратов, причем на хорошоокультуренной почве в большей степени. Произошли также изменения в содержании белкового и небелкового азота.
Внесение возрастающих доз тяжелых металлов привело к увеличению содержания аскорбиновой кислоты в растениях, причем на неокультуренной почве в большей степени. Интенсивный синтез витамина «С» можно объяснить, по-видимому, противодействием растительного организма стрессовой ситуации при возрастании доз тяжелых металлов, особенно на малобуферной неокультуренной дерново-подзолистой почве.
Таким образом, результаты проведенного опыта показали, что тяжелые металлы могут оказывать очень сильное и многостороннее влияние на химический состав растений и качество сельскохозяйственной продукции.
С целью изучения влияния различных факторов на поступление тяжелых металлов в растения в 1993 и 1994 годах в проектно-изыскательских станциях химизации системы агрохимслужбы проведены микрополевые и мелкоделяночные полевые опыты.
В ОПХ «Солянское» на выщелоченном черноземе проведен мелкоделяночный полевой опыт с картофелем. Выщелоченный среднемощный тяжелосуглинистый чернозем содержат 4% гумуса. фосфора — 290-271, калия — 125-132 мг/кг. Реакция среды в почве — близкая к нейтральной, гидролитическая кислотность — 3,14 мэкв на 100 г почвы. Содержание металлов в почве (мг/кг): меди — 22-29, цинка — 53-56, свинца — 19-22, кадмия -0.1 8-0.25. В навозе содержание тяжелых металлов было близко к почвенному (соответственно: 20,8; 47,5; 13,8 и 0,13 мг/кг). При внесении в почву солей тяжелых металлов их валовое содержание в среднем доведено до уровня (мг/кг): меди — 300, цинка — 1000, свинца — 200 и кадмия — 12. Минеральные, известковые удобрения, навоз и тяжелые металлы вносили в почву перед посадкой картофеля.
Результаты учета урожая показали, что тяжелые металлы оказали отрицательное влияние на урожай. Наименьшее снижение урожая наблюдалось на вариантах с известкованием почвы. Содержание меди в клубнях на всех вариантах менялось несущественно. Известкование снизило содержание этого металла до уровня контрольного варианта. Содержание цинка на варианте NPK + TM достигло уровня ПДК, а на варианте NPK + TM + навоз превысило его. Известкование существенно снизило содержание цинка в клубнях в 2-3 раза. Содержание свинца и кадмия в клубнях было значительно ниже предельнодопустимого уровня, но и на этих элементах (особенно на кадмии) проявилось действие известкования, снижающего их содержание (табл. 78).
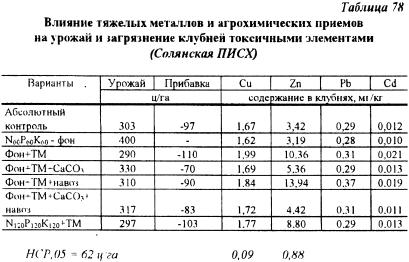
Таким образом, результаты опыта Солянской ПИСХ на выщелоченном черноземе показали, что даже в условиях сильного загрязнения почвы медью, цинком, свинцом и кадмием (одновременно путем внесения их воднорастворимых соединений) можно подучать клубни картофеля, соответствующие гигиеническим санитарным нормам Причем следует подчеркнуть высокую эффективность известкования почвы на черноземе с pH 5.6 и содержанием поглощенных кальция и магния 33 мэкв на 100 г. При известковании величина pH увеличивалась до 5,9-6,0. Действие органических удобрений на содержание тяжелых металлов проявилось слабо.
В опытах Тарской ПИСХ с картофелем на серой лесной среднекислой почве внесение 100 мг/кг почвы сернокислого цинка увеличило содержание этого элемента в клубнях с 5,2 до 7,8 мг/кг и ботве с 9,9 до 110 мг/кг. При известковании почвы (9,1 т/гa CaCO3) в сочетании с внесением сапропеля в дозе 200 т/га содержание цинка в клубнях и ботве снижалось до уровня фонового варианта.
В ПИЦАС »Волгоградский» проведены исследования токсичности тяжелых металлов в овощном севообороте на солонцовой почве (pH 8,3). Кадмий, цинк и свинец вносили из расчета 2 ПДК в почве. Независимо от варианта опыта содержание тяжелых металлов в капусте существенно не изменялось и было намного ниже предельно допустимой концентрации. Аналогичные данные получены и по свекле. Полученные результаты, по-видимому, главным образом связаны с щелочной реакцией солонца тяжелого гранулометрического состава.
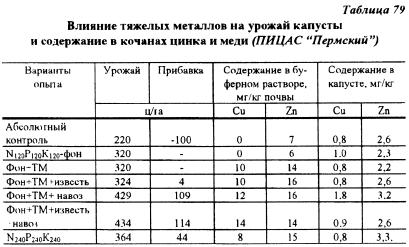
В ПИЦАС «Пермский» также проведен по аналогичной схеме опыт с капустой на дерново-подзолистой почве с близкой к нейтральной реакцией среды. На вариантах с TM совместно внесли цинк и медь из расчета 60 мг/кг почвы каждого элемента. Несмотря на резкое увеличение содержания подвижных форм меди и цинка в почве, содержание этих элементов в капусте существенно не изменялось (табл. 79), что, по-видимому, связано с нейтральной реакцией среды в почве. По этой же причине не проявилась влияние известкования на урожай, химический состав капусты и содержание подвижных форм меди и цинка в почве.
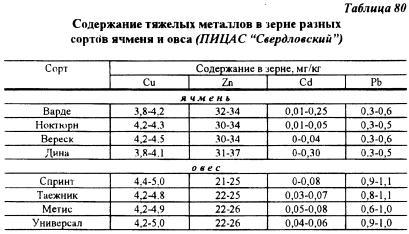
В ПИЦАС «Свердловский» проведено изучения влияния агрохимического окультуривания почв на содержание тяжелых металлов в четырех сортах овса и ячменя. В схеме опыта были варианты, в которых вносили 120 т/га навоза. 6 т/га извести и PK с целью доведения их содержания до 150 мг/кг почвы. Почва участка темно серая. pH 5,5-5,9. содержание фосфора — 28, калия — 100 мг/кг. степень насыщенности основаниями около 90%. Анализы растений показали, что содержание Cu, Zn, Pb и Cd в зерне во всех случаях было ниже ПДК и не зависело от применяемых удобрений (табл. 80). Существенных различий между сортами овса и ячменя по содержанию в зерне тяжелых металлов также не обнаружено.
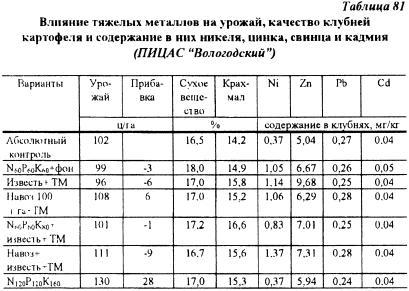
В ПИЦАС «Вологодский» проведен мелкоделяночный полевой опыт на дерново-подзолистой легкосуглинистой слабо-окультуренной почве (pH — 5,5, Hг — 1,6 мэкв, Ca + Mg — 3,7 мэкв, Р2О5 — 18,2 мг, K2O — 15 мг на 100 г почвы. Тяжелые металлы: цинк, свинец, кадмий и никель вносили в почву в виде водно-растворимых солей из расчета на чистый металл: цинка — 200. свинца — 60. кадмия — 2, никеля — 170 мг/кг почвы за 3 дня перед посадкой картофеля. В течение вегетации на вариантах с внесением тяжелых металлов наблюдалось отставание в прохождении картофелем биологических фаз развития. Результаты учета урожая показали, что отрицательное действие тяжелых металлов на урожай картофеля и основные показатели его качества не проявилась (табл. 81). Наоборот, содержание сухого вещества и крахмала при непосредственном внесении комплекса тяжелых металлов в воднорастворимой форме в клубнях повысилось. Существенных изменений в содержании свинца и кадмия при этом не было. Содержание цинка, и особенно никеля в клубнях увеличивалось, но находилась в интервале ниже ПДК.
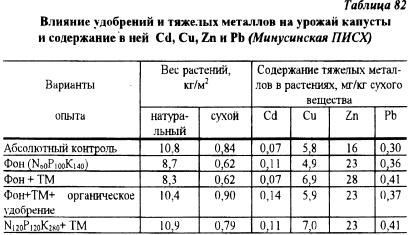
В степной зоне юга Красноярского края на Минусинской ПИСХ в 1994 году проведен мелкоделяночный полевой опыт по изучению влияния тяжелых металлов на урожай и качество капусты. Почва-чернозем обыкновенный маломощный малогумусный легкосуглинистый. Исходная агрохимическая характеристика почвы: содержание гумуса 2,4%. pH 7,6, подвижного фосфора 266 мг, обменного калия 171 мг/кг, обменных кальция 12,1 и магния 1,8 мэкв на 100 г почвы; содержание кадмия -0.03, меди — 11,4, цинка — 26,8, свинца — 6,6 мг/кг. В качестве органического удобрения в опыте применяли перегной в дозе 70 т/га. Тяжелые металлы вносили из расчета (мг/кг почвы): кадмий — 10, медь — 200, цинк — 600, свинец — 100. Результаты учета урожая, приведенные в таблице 82, показали, что содержание тяжелых металлов в кочанах капусты по всем вариантам опыта не превысило ПДК, несмотря на высокое содержание металлов в почве, тем более, что они были внесены непосредственно под капусту в воднорастворимой форме в виде растворов. Эти материалы свидетельствуют о вероятном наличии у капусты защитных механизмов, препятствующих поступлению тяжелых металлов в растения. Кроме этого определенную роль могли сыграть и свойства почвы, в основном нейтральная реакция среды, препятствующая загрязнению металлами овощной продукции.
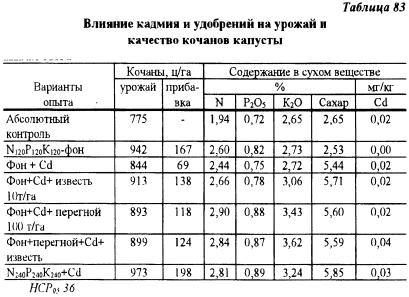
В ПИСХ «Марийская» проведен микрополевой опыт с капустой на дерново-подзолистой тяжелосуглинистой почве (pH — 5,8, гумус — 3,8%, P2O5 — 185, K2O — 90 мг/кг) с целью изучения влияния кадмия на урожай и химический состав капусты — сорта «Лосиноостровская». Посадка капусты произведена на второй день после заделки удобрений и соли кадмия в почву. Кадмий внесен в дозе 5 мг/кг почвы. Результаты учета урожая капусты показали, что внесение кадмия привело к его снижению с 942 до 844 ц/га. Известкование почвы и внесение перегноя уменьшили токсичность кадмия, а применение двойной дозы минеральных удобрений устранило его отрицательное влияние на урожай (табл. 83). Кадмий снижал также содержание азота и фосфора в капусте; известь, перегной и двойная доза удобрений повышали содержание этих питательных элементов. Содержание кадмия, за исключением предпоследнего варианта, было низким.
Таким образом, внесение кадмия в дозе 5 мг на кг почвы непосредственно перед посадкой капусты существенно не отразилось на качестве ее продукции.
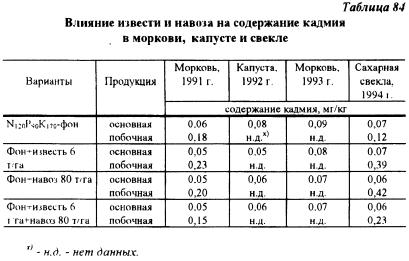
ПИЦАС «Московский» провел мелкоделяночные опыты в совхозе «Имени Моссовета» на загрязненной кадмием хорошо окультуренной дерново-подзолистой почве (pH 6,1), содержание гумуса 5,4%, P2O5 — более 1250, K2O — 324 мг/кг. Содержание кадмия в почве в среднем — около 4 мг/кг. Результаты одного из опытов, приведенные в таблице 84, показали, что даже на хорошо окультуренной почве применение известкования и органических удобрений заметно снизило содержание кадмия в корнеплодах моркови и кочанах капусты. В другом полевом опыте по изучению доз органических удобрений положительный эффект получен при внесении в почву не менее 100 т/га навоза.
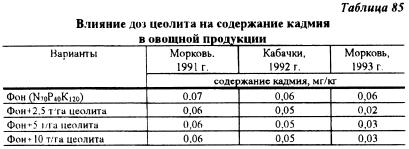
В полевом опыте с возрастающими дозами цеолита положительное влияние этого мелиоранта проявилось заметно на моркови на третий год последействия (табл. 85). В первые два года проведения опыта снижение содержания кадмия в моркови и кочанах от внесения цеолита было незначительным. Существенной разницы в эффективности между дозами цеолита не проявилось.
Таким образом, загрязнение растительной продукции тяжелыми металлами зависит от свойств металлов и их концентрации в почве, почвенных условий и биологических особенностей растений. Между этими главными факторами имеются сложные зависимости, для количественного описания которых с помощью математических методов в настоящее время крайне недостаточно экспериментального материала. Путем подбора устойчивых к загрязнению растений и целенаправленного изменения свойств почв можно снижать содержание тяжелых металлов в растениях. Однако, пределы ожидаемого содержания элементов в растительной продукции гарантировать пока нельзя.
Тяжелые металлы и их влияние на растения Текст научной статьи по специальности «Экологические биотехнологии»
Аннотация научной статьи по экологическим биотехнологиям, автор научной работы — Узаков З.З.
Постоянный рост народонаселения и быстрое развитие производства привели в конце XX-го века ситуацию с состоянием окружающей среды во многих странах и регионах мира на грань экологического кризиса. К числу основных факторов деградации природной среды относится ее загрязнение различными поллютантами, среди которых одно из главных мест занимают тяжелые металлы . В силу сказанного становится понятной актуальность исследований, посвященных влиянию тяжелых металлов на растения. В настоящее время они активно ведутся во многих странах мира.
Похожие темы научных работ по экологическим биотехнологиям , автор научной работы — Узаков З.З.
Текст научной работы на тему «Тяжелые металлы и их влияние на растения»
МЕЖДУНАРОДНЫЙ НАУЧНЫЙ ЖУРНАЛ «СИМВОЛ НАУКИ» № 1-2/2018 ISSN 2410-700Х
преподаватель, Каршинский государственный университет,
г. Карши, Узбекистан E-mail: uzakov.zafar@mail.ru
ТЯЖЕЛЫЕ МЕТАЛЛЫ И ИХ ВЛИЯНИЕ НА РАСТЕНИЯ
Постоянный рост народонаселения и быстрое развитие производства привели в конце XX-го века ситуацию с состоянием окружающей среды во многих странах и регионах мира на грань экологического кризиса. К числу основных факторов деградации природной среды относится ее загрязнение различными поллютантами, среди которых одно из главных мест занимают тяжелые металлы. В силу сказанного становится понятной актуальность исследований, посвященных влиянию тяжелых металлов на растения. В настоящее время они активно ведутся во многих странах мира.
Тяжелые металлы, природная, техногенная, почва, экология, химические элементы, ртуть,
свинец, кадмий, цинк, медь, мышьяк.
Термин «тяжелые металлы» был впервые употреблен еще в 1817 году немецким химиком Леопольдом Гмелиным (Leopold Gmelin), который разделил известные в то время химические элементы на три группы: неметаллы, легкие металлы и тяжелые металлы (Habashi, 2009).
Однако до сих пор не существует единого понимания, что же такое «тяжелые металлы». Более того, в техническом отчете IUPAC (International Union of Pure and Applied Chemistry — Международный союз теоретической и прикладной химии) за 2002 год отмечено, что термин «тяжелый металл» имеет неверное толкование из-за противоречивых определений. На сегодняшний день выделены лишь критерии, по которым определяется принадлежность того или иного химического элемента к данной группе. Среди них: плотность, атомный вес и атомное число. Словосочетание «тяжелые металлы» часто рассматривается с природоохранной точки зрения (Duffus, 2002), и тогда при включении элемента в эту группу учитываются не столько его физические и химические свойства, сколько биологическая активность, токсичность для живых организмов, распространенность в природной среде, степень вовлеченности в природные и техногенные циклы [1, с. 7].
Тяжелые металлы относятся преимущественно к рассеянным химическим элементам, поэтому загрязнению ими подвергается земная поверхность, в частности, почвенный покров и гидросфера, а также атмосфера (Добровольский, 1983, 2004). В силу этого повышение их концентрации в окружающей среде вследствие естественного или антропогенного поступления может носить глобальный характер. К естественным источникам тяжелых металлов относятся горные породы (из продуктов, выветривания которых сформировался почвенный покров), вулканы, космическая пыль, эрозия почв, испарение с поверхности морей и океанов, выделение их растительностью (Кабата-Пендиас, Пендиас, 1989; Добровольский, 1992; Богдановский, 1994) [1, с. 9].
Тяжелые металлы (ртуть, свинец, кадмий, цинк, медь, мышьяк) относятся к числу распространенных и весьма токсичных загрязняющих веществ. Они широко применяются в различных промышленных производствах, поэтому, несмотря на очистные мероприятия, содержание соединения тяжелых металлов в промышленных сточных водах довольно высокое. Прежде всего, представляют интерес те металлы, которые наиболее широко и в значительных объемах используются в производственной деятельности и в результате накопления во внешней среде представляют серьезную опасность с точки зрения их биологической активности и токсических свойств. К таким тяжелым металлам относятся свинец, ртуть,
МЕЖДУНАРОДНЫЙ НАУЧНЫЙ ЖУРНАЛ «СИМВОЛ НАУКИ» № 1-2/2018 ISSN 2410-700Х кадмий, цинк, висмут, кобальт, никель, медь, олово, сурьма, ванадий, марганец, хром, молибден и мышьяк.
Многие тяжелые металлы относятся к микроэлементам. То есть химическим элементам, присутствующим в организмах в низких концентрациях (обычно тысячные доли процента и ниже).
Значительное количество химических элементов, постоянно обнаруживаемых в организмах, оказывает определенное влияние на течение процессов обмена веществ и на ряд физиологических функций. Количественное содержание биоэлементов, входящих в состав организмов, сильно варьирует в зависимости от среды обитания, способа питания, видовой принадлежности и т. п. Помимо общего благоприятного влияния на процессы роста и развития, установлено специфическое воздействие ряда микроэлементов на важнейшие физиологические процессы — например, фотосинтез у растений. [2, с. 13]
При увеличении содержания металлов в почве снижается её общая биологическая активность, и это резко отражается на росте и развитии растений, причём разные растения реагируют на избыток металлов по-разному. Металлы распределяются по органам растений неравномерно. В наибольшей степени металлы накапливаются в листьях. Это обусловлено многими причинами, одна из которых — локальное накопление металлов в результате перехода их в малоподвижную форму. Например, в случае медной интоксикации окраска некоторых листьев у растений изменяется до красной и буро-коричневой, что свидетельствовало о разрушении хлорофилла.
Токсичность тяжелых металлов связана с их физико-химическими свойствами, со способностью к образованию прочных соединений с рядом функциональных группировок на поверхности и внутри клеток. Симптомы «отравления» растений тяжелыми металлами внешне проявляются в замедлении их роста и развития, изменении цвета и увядании листьев, уродливости и недоразвитости корневой системы.
Реакция растений на повышенные концентрации тяжёлых металлов (концентрация в почве, мг/кг):
Pb (100-500). Ингибирование дыхания и подавление процесса фотосинтеза, иногда увеличение содержания кадмия и снижение поступления цинка, кальция, фосфора, серы, снижение урожайности, ухудшение качества растениеводческой продукции. Внешние симптомы — появление темно-зеленых листьев, скручивание старых листьев, чахлая листва.
Cd (1-13). Нарушение активности ферментов, процессов транспирации и фиксации СО2, торможение фотосинтеза, ингибирование биологического восстановления NO2 до NO, затруднение поступления и метаболизма в растениях ряда элементов питания. Внешние симптомы — задержка роста, повреждение корневой системы, хлороз листьев.
Zn (140-250). Хлороз молодых листьев.
Cr (200-500).Ухудшение роста и развития растений, увядание надземной части, повреждение корневой системы, хлороз молодых листьев, резкое снижение содержания в растениях большинства незаменимых макро и микроэлементов (К, Р, Fe, Mn, Cu, B и др.).
Ni (30-100). Подавление процессов фотосинтеза и транспирации. При этом наблюдаются явления эндемического заболевания растений, например уродливые формы. Типичные симптомы повреждающего токсического действия никеля: хлороз, появление желтого окрашивания с последующим некрозом, остановка роста корней и появления молодых побегов или ростков, деформация частей растения, необычная пятнистость, в некоторых случаях — гибель всего растения. [2, с. 33].
Список использованной литературы:
1. Титов А.Ф., Казнина Н.М., Таланова В.В. Тяжелые металлы и растения. Петрозаводск: Карельский научный центр РАН, 2014. 194 с.
2. СЛ. Давыдова, В.И. Тагасов Тяжелые металлы как супертоксиканты XXI века: Учеб. пособие. — М.: Изд-во РУДН, 2002. — 140 с.
Фитотоксичное действие тяжелых металлов при техногенном загрязнении окружающей среды

Байсеитова, Н. М. Фитотоксичное действие тяжелых металлов при техногенном загрязнении окружающей среды / Н. М. Байсеитова, Х. М. Сартаева. — Текст : непосредственный // Молодой ученый. — 2014. — № 2 (61). — С. 382-384. — URL: https://moluch.ru/archive/61/8882/ (дата обращения: 05.07.2022).
В работе описаны загрязнение окружающей среды тяжелыми металлами, распространение и аккумуляция металлов в природной среде и их негативные воздействия на растения.
The pollution plumbum producing plant is influence on heavy metals accumulation processing of plants. Theheavymetalswillbechangedofplantsgename.
Основными источниками антропогенного поступления тяжелых металлов в окружающую среду являются металлургические предприятия, тепловые электростанции, карьеры и шахты по добыче полиметаллических руд, транспорт, химические средства защиты сельскохозяйственных культур от болезней и вредителей, сжигание нефти и различных отходов и пр. Наиболее мощные ореолы тяжелых металлов возникают вокруг предприятий черной и особенно цветной металлургии в результате атмосферных выбросов. Действие загрязняющих веществ распространяется на десятки километров от источника поступления элементов в атмосферу. По приведенным ниже данным можно судить о размерах антропогенной деятельности человека: вклад техногенного свинца составляет 94–97 %(остальное природные источники)., кадмия-84–89 %процентов, меди-56–87 %, никеля-66–75 %, ртути -58 % [1,2].
Заметное загрязнение атмосферного воздуха и почвы происходит за счет транспорта, в том числе авиационного. Большинство тяжелых металлов, содержащихся в пылегазовых выбросах промышленных предприятий, как правило, более растворимы, чем природные соединения [3].
Тяжелые металлы — это группа химических элементов с относительной атомной массой более 40. Появление в литературе термина «Тяжелые металлы» было связано с проявлением токсичности некоторых металлов и опасности их для живых организмов. Однако в эту группу вошли и некоторые микроэлементы, жизненная необходимость и широкий спектр биологического действия которых неопровержимо доказаны. Влияние микроэлементов на жизнедеятельность животных и человека активно изучается и в медицинских целях. В настоящее время выявлено, что многие заболевания, синдромы и патологические состояние вызваны дефицитом, избытком и дисбалансом микроэлементов в живом организме и имеют общее название «микроэлементы».
Фитотоксичное действие тяжелых металлов проявляется, как правило, при высоком уровне техногенного загрязнения ими почв и во многом зависит от свойсв и особенностей поведения конкретного металла. Однако в природе ионы металлов редко встречаются изолированно друг от друга. Поэтому разнообразные комбинативные сочетания и концентрации разных металлов в среде приводят к изменениям свойств отдельных элементов в результате их антогонического воздействия на живые организмы [4].
Растительная пища является основным источником поступления ТМ организм человека и животных. По данным с ней поступают 40–80 % тяжелых металлов, и только 20–40 %. — с воздухом и водой. Поэтому от уровня накопления тяжелых металлов в растениях, используемых в пищу, в значительной степени зависит здоровье населения. Химический состав растений, как известно, отражает элементный состав почв. Поэтому избыточное накопление тяжелых металлов растениями обусловлено, прежде всего, их высокими концентрациями в почвах.
Несмотря на существенную изменчивость различных растений к накоплению тяжелых металлов, биоаккумуляция элементов имеет определенную тенденцию, позволяющую упорядочить их в несколько групп: 1) Cd,Cs, Rb — элементы интенсивного поглощения; 2) Zn, Mo, Cu, Pb, Co, As –средней степени поглощения; 3) Mn, Ni, Cr –слабого поглощения; 4) Se, Fe, Ba, Te — элементы труднодоступные растениям.
Другой путь поступления тяжелых металлов в растения — некорневое поглощение из воздушных потоков. Поступление элементов в растения через листья (или фолиярное поглощение) происходит, главным образом, путем неметаболического проникновения через кутикулу. Тяжелые металлы, поглощенные листьями могут переносится в другие органы и ткани и включаться в обмен веществ.
Свинец и кадмий относятся высокотоксичным металлам. В придорожных растениях количество свинца резко повышено, оно в 10–100 раз выше по сравнению с растениями, растущими вдали от дорог. Между содержанием свинца в растениях и расстоянием дерева от дороги существует доказуемая обратная зависимость. Свинец в достаточно высокой концентрации тормозит прорастание семян растений, замедляет рост корней в длину, а также образование корневых волосков. Листья отравленных свинцом растений становятся хлоротичными в межжилковых зонах. Особенно сильно поражаются молодые листья. Высокое содержание свинца в растениях негативно влияет на рост и развитие:
— снижается активность фотосистемы І и ІІ, причем фотосистема-ІІ более чувствительная к действию этого фитотоксиканта.
— оказывает ингибирующее влияние на реакцию Хилла, т. е. на способность изолированных хлоропластов на свету выделять кислород.
— в хлорпластах растений наблюдается подавление образования АТФ;
— вызывает потерю тургора клетками растений;
— прекращается деление клеток корня;
— подавляется образования корнеплодов, урожайность культурных растений;
— снижается количество каротина и аскорбиновой кислоты;
Некоторые травянистые растения, чувствительны по отношению к свинцу: ячмень, овес, пшеница, картофель. Среди дикорастущих следует отметить смолевку, которая от высокого содержания свинца приобретает карликовую форму, листья и стебли становятся темно-красными, а цветки мелкими и невзрачными [5].
Главным загрязнителем окружающей среды кадмием является цветная металлургия и обработка цветных металлов. Кроме того кадмий поступает в атмосферу при сгорании мусора и отходов. Большое количество кадмия обнаруживается в растения, произрастающих поблизости от автодорог. Так, например в хвое ели обыкновенной, растущей поблизости автодорог количество кадмия возрастает в 11–17 раз. Симптомы избыточного поступления в растения кадмия проявляются в постепенном изменении окраски кончиков листьев и черешков до красновато-бурой и пурпурной. При этом листья скручиваются и опадают. Кадмий замедляет темпы роста растений. При внесении его в количестве 20 мг на 1 кг почвы урожай растения снижался на 50 %. По силе своего действия кадмий превосходит многие другие тяжелые металлы. Гибель растений отмечается при концентрации кадмия в почве в количестве 30 мг/кг и выше. Большое количество кадмия поступает в почву при разработке и добыче цинковых руд. На таких почвах нельзя выращивать растения, ибо этот токсикант аккумулируется в тканях растений и может затем поступать в организм человека. Накопления кадмия происходит главным организм человека. Одна из причин торможения роста растений, произрастающих в присутствии кадмия — резкое ослабление интенсивности фотосинтеза. Присутствие в 1 кг листьев 96 мг этого элемента снижает интенсивность фотосинтеза на 50 % [6].
Поступление тяжелых металлов в растения может происходить непосредственно из воздуха с оседающей на листья и хвою пылью и транслокации из почвы: доля тяжелых металлов в составе пыли на поверхности листьев вблизи источника составляет в среднем 30 проц. от общего содержания в них тяжелых металлов. В понижениях и с наветренной стороны это доля может доходить до 60 %. По мере удаления от источника роль атмосферного загрязнения заметно уменьшается.
Главным загрязнителем атмосферы кадмием является цветная металлургия и обработка цветных металлов. Кроме того, кадмий поступает в окружающую среду при сгорании некоторых видов топлива и особенно при сжигании мусора и отходов. Из атмосферы кадмий поступает в почву. Загрязнение ее этим элементом носит устойчивый характер, поскольку из почвы он вымывается медленно. Большое количество кадмия обнаруживается в растения, произрастающих поблизости от автомобильных дорог. Так, например в хвое ели обыкновенной, растущей поблизости от автострад, количество кадмия возрастает в 11–17 раз. Симптомы избыточного поступления в растения кадмия проявляются в постепенном изменении окраски кончиков листьев и черешков до красновато-бурой и пурпурной. При этом листья скручиваются и становятся хлоратичными и опадают. По силе своего действия на растения кадмий превосходит многие другие тяжелые металлы. Гибель растений отмечается при концентрации этого элемента в почве в количестве 30 мг/кг. Вблизи предприятий, выбрасывающих в атмосферу кадмий наблюдается резкое снижение урожайности и даже гибель культурных растений. Накопление кадмия происходит главным образом в корнях растений (риса, пшеницы), однако часть его достигает органов. Одна из причин торможения роста растений, произрастающих в присутствии кадмия, резкое ослабление интенсивности фотосинтеза. Присутствие в 1 кг листьев 96 мг этого элемента снижает интенсивность фотосинтеза на 50 %. Существует прямая зависимость между содержанием кадмия в почве и поступлением его в растения.
Токсическое влияние оказывают на растения и другие металлы, загрязняющие природную среду, например бериллий, марганец, медь, хром, ванадий, цинк и др.
1. Кузнецов А. В. Контроль техногенного загрязнения почв и растений // Агрохимический вестник. –1997г. -№ 5, -С. 7–9
2. Минеев В. Г. Проблема тяжелых металлов в современном земледелии // Тяжелые металлы и радионуклиды. –М., 1994г. –С. 42–48
3. Бутовский Р. О. Тяжелые металлы как техногенные химические загрязнители и их токсичность для почвенных беспозвоночных животных //Агрохимия.-2005 г. -№ 4, -С 73–91.
4. Алексеев Ю. В. Тяжелые металлы в почвах и растениях. –Ленинград, 1987 г. –С. 141–144.
5. Зырин Н. Г. Тяжелые металлы в почвах и растениях в районе медеплавильного завода. –м., 1986г. –С. 81
6. Артомонов В. И. Растения и чистота природной среды. –М., 1986 г. –С. 27–31.
Основные термины (генерируются автоматически): металл, растение, кадмий, окружающая среда, почва, лист, организм человека, цветная металлургия, элемент, главный образ.
Источник http://milk-industry.ru/praktikum-po-agrohimii/4081-tyazhelye-metally-v-rasteniyah.html
Источник https://cyberleninka.ru/article/n/tyazhelye-metally-i-ih-vliyanie-na-rasteniya
Источник https://moluch.ru/archive/61/8882/